使用搭载waters_connect™信息学软件的BioAccord™ LC-MS系统分析合成寡核苷酸中杂质的工作流程
摘要
随着合成寡核苷酸作为治疗药物受到越来越多的关注,特别是在进入研发流程的新型药物形式在长度和复杂性上不断增加的情况下,开发能够测定其杂质谱的有效方法至关重要。目前用于杂质分析的既有HPLC-MS(单四极杆)方法非常耗时,并且需要手动处理步骤,存在引入人为误差的风险,在受监管的环境中难以实施。为应对这些挑战,沃特世公司开发了寡核苷酸杂质分析工作流程数据包。该工作流程的开发基于BioAccord系统,这是一款UPLC-Tof MS,速度更快、性能更稳定、分离度更高,可为分析检测带来更高的质量分辨率和灵敏度。工作流程中包含的方法均附带现成的计算和报告模板,可自动化完成许多数据分析步骤,并简化少数仍然需要用户输入的步骤,从而精简整个分析流程。这些工具和培训数据集可减轻用户负担,促进合成寡核苷酸杂质谱的分析。
优势
- 精简的工作流程,数据分析时间从数小时缩短至数分钟
- waters_connect信息学软件可进行自动化、合规的数据处理,减少手动分析引入人为误差的风险
- 方法简便易用且易于调整,减轻培训负担,并降低在执行常规方法操作时,对用户所需专业知识的要求
- 相较于传统的单四极杆MS平台,BioAccord系统或Xevo QTof MS具有更出色的色谱和质谱性能1
简介
近年来,随着人们开始探索新型药物产品形式,核酸治疗药物引起了广泛关注。这类治疗药物包括合成寡核苷酸,这是一种通过保护、偶联和去保护反应的循环过程合成的短核酸链。虽然寡核苷酸因能够选择性地靶向特定基因而发挥重要作用,但其合成过程中会引入杂质,对有效性和安全性造成影响。随着合成寡核苷酸的长度和复杂性增加,杂质谱的复杂性也随之增加,这可能会给产品杂质组分的评估带来挑战1。
目前已经建立了一些用于测量合成寡核苷酸产品中所含杂质的方法。然而,这些方法在实施过程中都存在特定的挑战。通常情况下,杂质表征是在单四极杆质谱仪上进行的。这种仪器虽然操作复杂,但已被证明对简单短链寡核苷酸的分析是有效的。而进入开发流程的新型药物需要更先进的LC-MS分析系统,这些分析系统必须提供足够的灵敏度和分辨率,能够对近乎同分异构的杂质组分实现质量分离,并对低浓度杂质进行定量。因此,改用飞行时间(Tof)检测器(例如BioAccord系统或Xevo QTof MS)将非常有利,因为它可以提高分析能力并简化用户操作2。 数据分析同样存在挑战,因为现有工作流程在数据处理过程中通常需要人工干预。这一过程不仅耗时,还存在与潜在人为误差相关的风险。因此,这些方法难以在受监管的实验室环境中执行。
为应对这些挑战,本文详细介绍了一种全新发布的专为合成寡核苷酸杂质分析而设计的工作流程。本文所述的工作流程使用配备ACQUITY Premier LC的BioAccord系统,以短梯度进行数据采集,可提高通量,并尽可能减少溶剂消耗和危险废液的产生。使用waters_connect信息学平台的UNIFI应用程序进行数据分析,自动化完成数据采集、处理和报告流程,从而简化对采集数据的分析。数据分析包含两个工作流程,如图1所示,分别考虑了寡核苷酸中的预期杂质和非预期杂质。

实验
样品描述
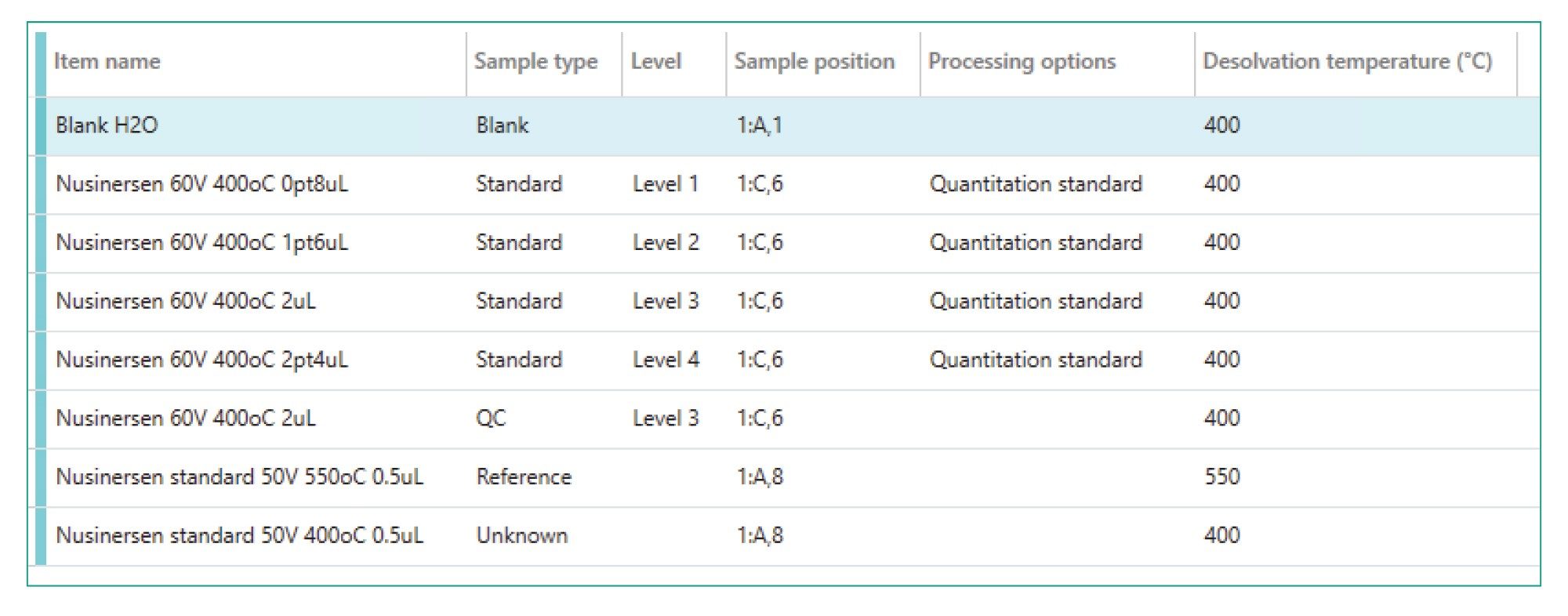
用纯水稀释诺西那生(Nusinersen),并以不同体积进样至色谱柱,建立标准曲线,柱上进样量范围为0.8 µg~2.4 µg。我们平行采集了两份样品,一份使用较温和的电离条件(400 °C),另一份使用较恶劣的电离条件(550 °C)。样品组示例如图2所示。
诺西那生的序列为U-*C-A-*C-*U-*U-*U-*C-A-*U-A-A-*U-G-*C-*U-G-G(甲基化位于“C”和“U”上),精确质量数为7122.2763 Da。
方法条件
液相色谱条件
|
液相色谱系统: |
ACQUITY™ Premier(二元) |
|
检测: |
ACQUITY Premier TUV;λ = 260 nm |
|
样品瓶: |
采用MaxPeak HPS的QuanRecovery样品瓶(部件号:186009186) |
|
色谱柱: |
ACQUITY Premier C18寡核苷酸分析专用柱(130 Å, 1.7 µm, 2.1 x 50 mm)(P/N:186009484) |
|
柱温: |
50 °C |
|
样品温度: |
6 °C |
|
进样体积: |
0.5-2.4 µL |
|
流速: |
0.250 mL/min |
|
流动相A: |
5 mM TBuAA;1 µM EDTA;水:乙腈90:10 |
|
流动相B: |
5 mM TBuAA;1 µM EDTA;水:乙腈20:80 |
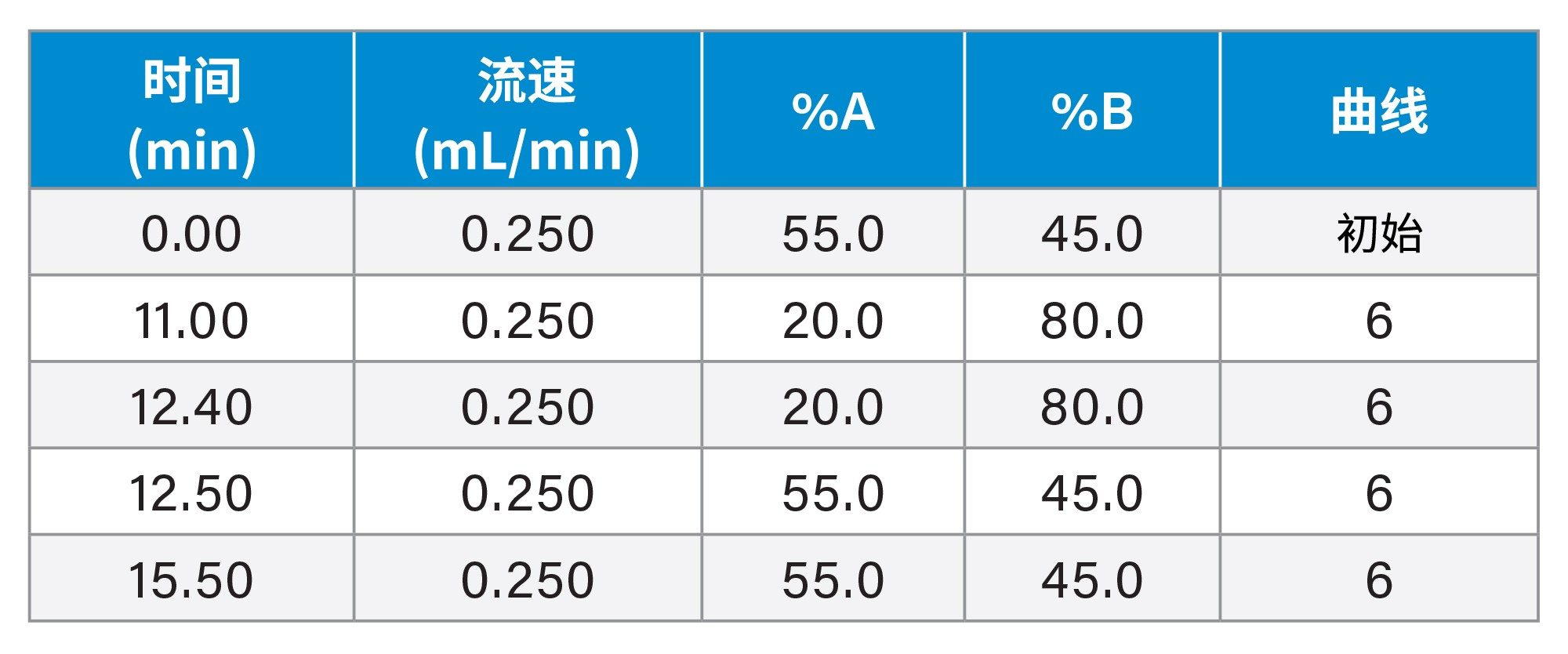
梯度表
质谱条件
|
质谱系统: |
ACQUITY RDa™检测器 |
|
电离模式: |
ESI,负离子 |
|
采集范围: |
高(400~5000 m/z) |
|
毛细管电压: |
0.80 kV |
|
锥孔电压: |
50 V |
|
脱溶剂气温度: |
温和条件:400 °C 恶劣条件:550 °C |
|
智能数据捕获: |
开 |
数据管理
使用waters_connect信息学平台(3.2.0版)的2D Quan和一体化UNIFI应用程序(3.6.0.21版)的精确质量数筛查工作流程采集和处理数据。
结果与讨论
在寡核苷酸的杂质表征中,数据分析所需的时间一直都是一大瓶颈,尤其是在需要对数据分析软件自动执行的步骤进行手动补充时。目前,在合成寡核苷酸的杂质分析中,广泛采用的方法是最初由Ionis Pharmaceuticals开发的HPLC离子对RP-UV-单四极杆方法3。 该方法虽然已被证明对简单的寡核苷酸适用,但它需要手动分析步骤,并且对于评估更长、更复杂的新一代寡核苷酸缺乏分析能力。
随着寡核苷酸产品线不断增加与发展,为满足由此衍生出的支持需求,我们开发出一种采用飞行时间质谱检测的UPLC方法。ACQUITY Premier UPLC系统能够缩短UPLC分离时间,减少溶剂消耗,并减少由此产生的有毒废液,同时提高分离质量和分析通量。BioAccord系统能够提供高分辨率质谱检测,在杂质分配过程中减少质量数测量误差,并改善近乎同分异构的杂质的检测。例如,序列杂质n-U和n-C的质量数仅相差约1 Da。在-4电荷态下,其m/z值(分别为1681.0468和1681.2928)非常接近,单四极杆MS无法区分,但可以通过BioAccord 系统上的Tof检测轻松区分。
此外,传统的Ionis方法有多个步骤需要用户手动输入,因此通量有限。由于依赖人工干预,该方法不仅耗时,还难以训练,在受监管的环境中难以实施。新用户需要接受大量培训(通常需要数周至数月)才能熟练掌握传统方法,并且依赖手动数据处理增加了与人为误差相关的风险。
新的寡核苷酸杂质分析工作流程通过自动化执行多个数据分析步骤,并简化少数仍需要用户输入的步骤,从而优化数据分析流程,缩短时间、降低出错风险并减少用户培训需求。借助这种自动化数据处理方法,过去需要一天时间才能处理的数据集,现在只需不到一个小时即可完成审查。数据包随附的默认分析方法可轻松适应不同全长产物及其相关杂质。
数据处理方法包括两个关键工作流程,分别标记为“靶向”和“非靶向”工作流程。靶向工作流程包括以下步骤:系统适应性、重复性检查、生成标准曲线、对从全长产物(FLP)中色谱分离的杂质进行UV积分,以及审查与FLP共流出的指定杂质的提取离子流色谱图(XIC)积分。非靶向工作流程包括用于确认FLP鉴定的系统适应性测试(基于质量数和钠加合物水平),以及审查与FLP共流出的所有未知杂质的XIC积分。
总而言之,如图1所示,这两种工作流程均能够与BioAccord LC-MS仪器上采集的单个数据集无缝协作,利用ACQUITY Premier UPLC系统和ACQUITY Premier寡核苷酸分析专用柱的色谱性能,提高分离速度(耗时只有传统HPLC-SQ方法的一半),同时相应地减少溶剂的使用量以及危险废液的产生(这是本分析中使用的溶剂和有毒含氟离子对试剂所面临的一项关键挑战),从而优化杂质分离。
靶向杂质分析工作流程
靶向工作流程包含通过系统适应性检查分析数据质量,以及使用UNIFI应用程序内的“定量检测Tof 2D色谱工作流程”,根据UV或MS数据对杂质峰进行积分。在该工作流程的第一步,用户可以选择手动调整UV积分。寡核苷酸通常表现出明显的峰拖尾(使用Premier UPLC系统和寡核苷酸分析专用填料可显著减少),因此难以确定合适的积分垂线。按照既定标准方法,FLP积分的截止点应基于最后一个与FLP共洗脱的杂质的保留时间确定3。 此工作流程步骤将根据这些标准计算截止点,并报告该值。用户只需手动将UV垂线调整为报告的截止点即可。
该工作流程的下一步是基于单一浓度的工作标准溶液(WSS)重复进样评估进样重复性。此引导式数据审查步骤以表格形式显示每次进样的FLP UV峰的相关信息,例如观测保留时间、UV响应和计算浓度。表格底部显示了每个值的平均值和%相对标准偏差(RSD)。这些信息可用于评估仪器性能和数据质量。
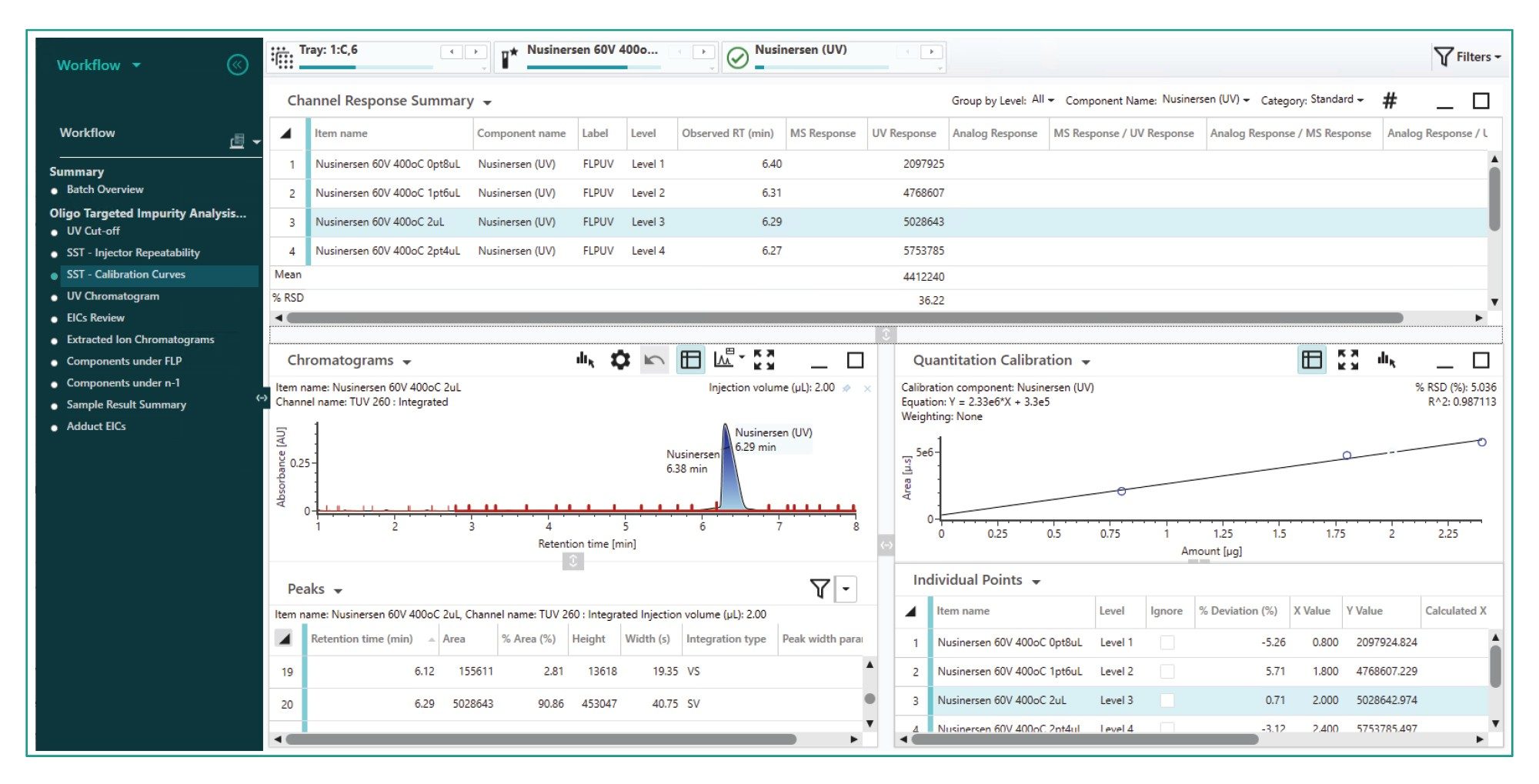
同样,下一步引导式数据审查步骤将展示不同浓度WSS进样生成的标准曲线,以确保对结果进行适当定量。根据UV和MS数据生成标准曲线,并报告每条曲线的趋势线方程和R2值。图3所示为工作流程中标准曲线审查步骤的屏幕截图。该方法包含限值检查,用于标记任何值超出可接受标准的结果。
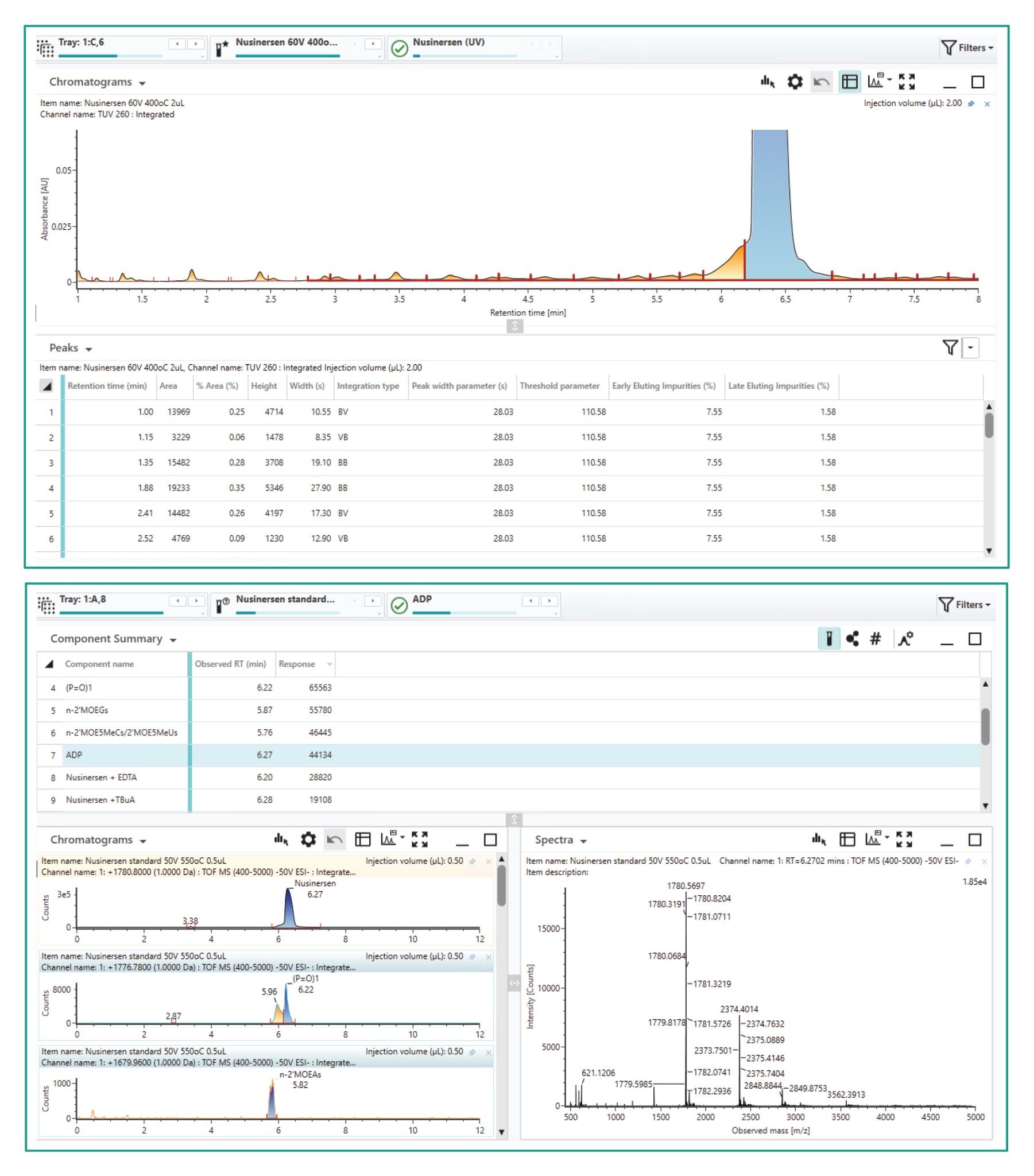
接下来的三个引导式数据审查步骤分别对UV通道和MS通道进行峰积分,如图4所示。通过UV积分对从FLP中色谱分离的峰进行定量。这些峰在色谱图中以黄色显示(图4,左侧),其保留时间、峰面积和相对峰面积(%)报告在色谱图下方的表中。表中还包括先洗脱(FLP之前)和后洗脱(FLP之后)峰的峰面积百分比总和,可用于纯度计算。
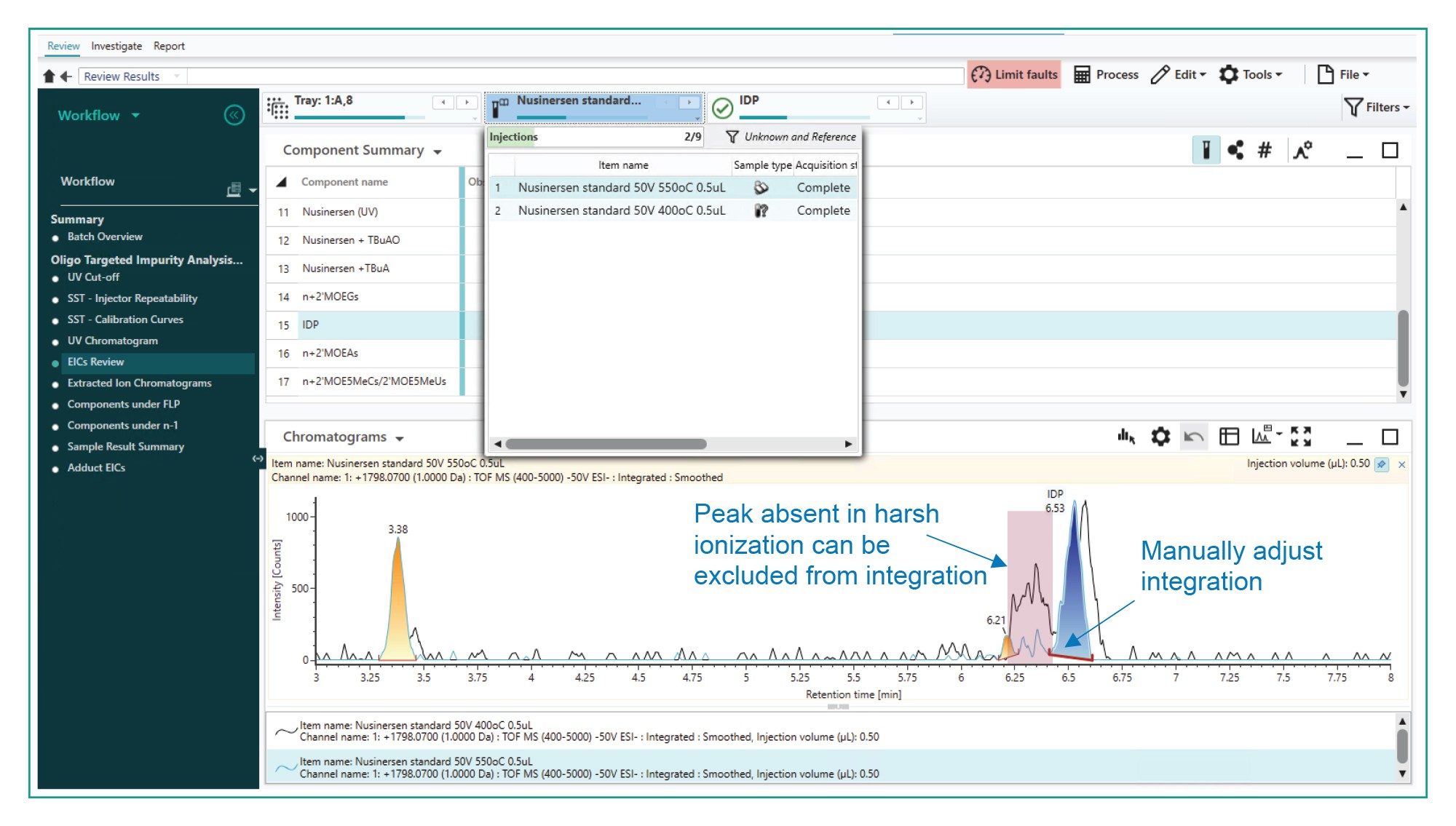
接下来的引导式审查步骤可以审查与FLP共洗脱的杂质峰的XIC积分,这些杂质峰已包含在目标组分列表中。通过此步骤,可以比较在较温和的电离条件和较恶劣的电离条件下采集的进样中的峰。电离过程中通常会产生加合物。如果加合物是未知的,它们可能会被误认为杂质。为了区分加合物峰与杂质峰,通常在较恶劣的条件下电离样品(例如使用更高的脱溶剂气温度)。在这种较恶劣的条件下,加合物会释出,因此通过比较更温和与更恶劣条件下的峰,揭示加合物对具有相同m/z的杂质的贡献情况。
虽然手动比较两种条件下的峰可能非常耗时,但该工作流程支持叠加比较两次进样,从而简化了这一步,如图5所示。在这一步,通过已知杂质m/z所对应的XIC,可以观察到恶劣电离条件与温和电离条件之间的差异。通过叠加两次进样可以看出,恶劣电离条件下的进样有部分峰缺失,而其余峰持续存在。在恶劣条件下的进样中缺失的部分峰,可能是与杂质具有相同m/z的加合物,因此可以从积分中剔除。因此,杂质的峰面积百分比更低,更能代表样品中的实际杂质含量。审查列表中的各指定杂质并根据需要手动调整后,每个峰的XIC积分结果将显示在接下来的引导式数据审查工作流程步骤中(图5右侧)。
最后的四个引导式数据审查工作流程步骤根据杂质类型(如目标组分列表中的标签所示)对杂质和加合物进行分组,并汇总多次进样得到的平均含量。
非靶向(共洗脱未知物)杂质分析工作流程
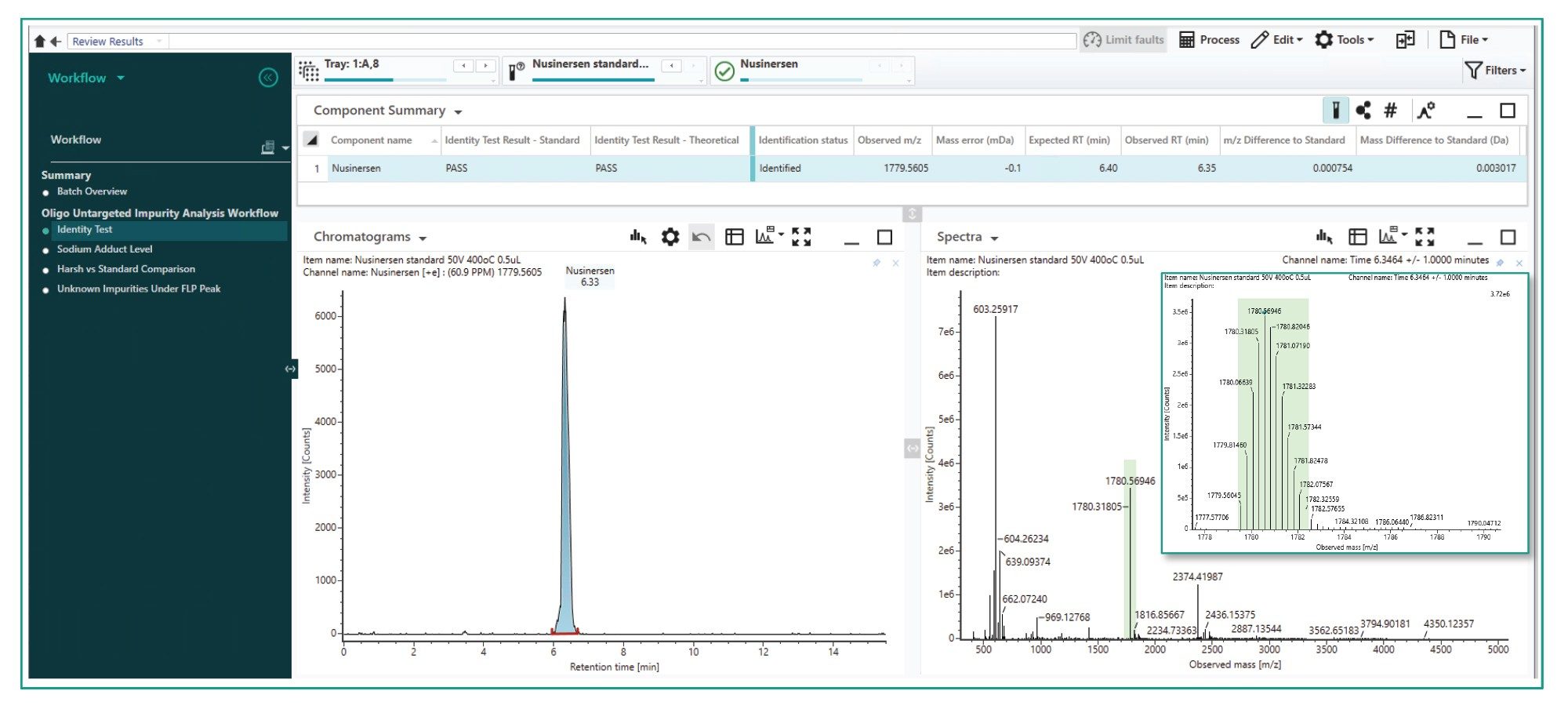
非靶向工作流程利用UNIFI应用程序中的精确质量数筛查工作流程执行额外的系统适应性测试,并根据与FLP共洗脱的未知杂质的汇总XIC对其进行定量分析。该引导式数据审查工作流程的第一个步骤是鉴定测试,通过比较样品的实测m/z与WSS进样中相同FLP的m/z或非靶向组分列表中标注的理论值,确认FLP的鉴定结果。如果m/z差异小于指定阈值(例如此处的0.2 m/z),则测试通过。该步骤还显示了FLP XIC和MS谱图,其中同位素峰簇以绿色突出显示(图6)。
钠加合物测试的作用原理与之类似,如果FLP钠加合物峰的相对强度与FLP峰相比小于指定阈值(例如,此处为3%),则测试通过。用户可以在方法中轻松编辑这两项测试的阈值。
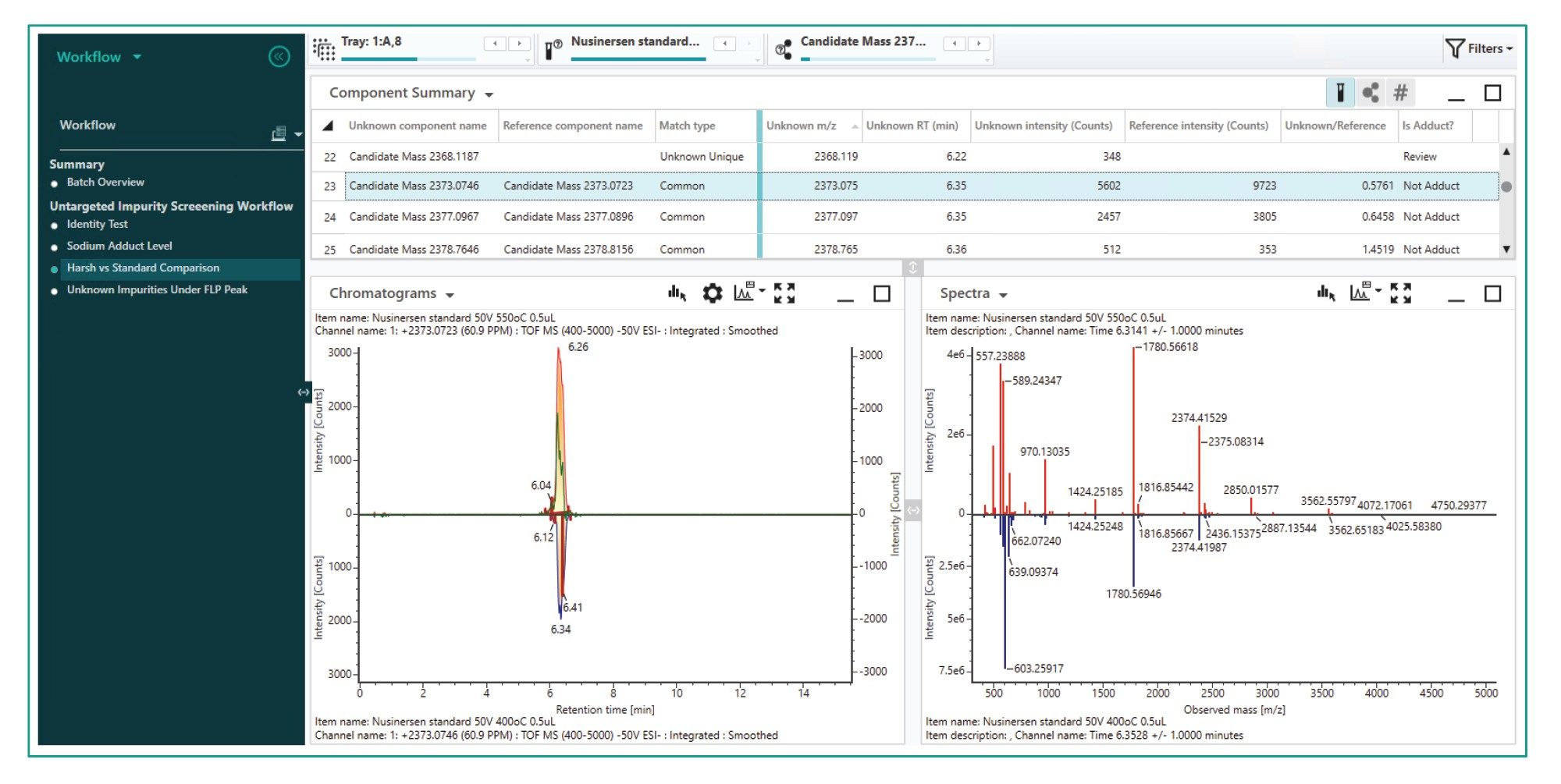
与靶向工作流程类似,非靶向工作工作流程也支持用户通过比较温和电离条件和恶劣电离条件来区分杂质峰和加合物峰。图7显示了温和电离条件与恶劣电离条件下所得XIC色谱图和质谱的镜像图。色谱图中的绿色迹线指示出差异,使用户能够轻松查看哪部分峰(如果有)来自加合物。然后即可对积分进行相应的手动更改。
引导式数据审查工作流程的最后一步列出了检出的所有与FLP共流出的未知杂质,并显示了这些杂质的质谱和XIC积分用于定量分析。只有相对强度高于指定检测阈值的杂质才会包含在此列表中(例如,在本例中,m/z低于FLP的相对强度为0.2%;m/z高于FLP的相对强度为0.3%)。为避免重复计数,此列表排除了所有从FLP中色谱分离或在组分列表中列为指定杂质的杂质。
报告模板
寡核苷酸杂质分析工作流程数据包还包含报告模板,以清晰、简洁的方式系统性汇总数据,以便快速交流数据和结果。靶向和非靶向工作流程各自生成报告。非靶向工作流程的示例报告页面(图8)中有一个标题页显示分析的基本信息,后跟该工作流程生成的系统适应性信息摘要。其他页面显示了与杂质定量相关的信息,例如通过表格列出所有检出杂质及其相对响应。最终报告部分包含用于数据质量验证的信息,例如每种定量杂质的XIC。

结论
随着合成寡核苷酸作为治疗药物引起越来越多的关注,因此需要新的分析方法,快速、可靠地分析复杂的杂质谱。减少手动数据分析是提高通量和降低人为误差风险的关键。我们的方法是通过更新工作流程实现自动化数据处理,弥补既有HPLC-单四极杆MS方法的短板。此数据包是使用waters_connect中的合规UNIFI应用程序,在UPLC-Tof MS系统上开发的。整体数据包可自动化完成极大部分数据分析工作,并引导用户轻松执行仍需要手动干预的步骤。这些一体化的引导式数据审查工作流程步骤将引导用户完成数据分析的每一环,内置的报告模板可将大量数据提炼为清晰、简明的表格和图像,以便快速交流。该工作流程包经过精心设计,可轻松适用于不同的合成寡核苷酸产品和杂质,减少了为每种新分子耗时进行方法开发的挑战。最终,新一代寡核苷酸将需要本应用纪要中所讨论的工具和方法。
参考资料
- Pourshashian S. Therapeutic Oligonucleotides, Impurities, Degradants, and Their Characterization by Mass Spectrometry.Mass Spectrom Rev. 2019 Dec, 40(2), 75–109.
- Doneanu CE, Knowles C, Fox J, Harry E, Yu YQ, Fredette J, Chen W. 使⽤装配ACQUITY Premier产品的BioAccord LC-MS系统分析寡核苷酸杂质.沃特世应用纪要.2021年7月; 720007301ZH.
- Rentel C, Gaus H, Bradley K, Luu N, Kolkey K, Mai B, Madsen M, Pearce M, Bock B, Capaldi D. Assay, Purity, and Impurity Profile of Phosphorothioate Oligonucleotide Therapeutics by Ion Pair-HPLC-MS.Nucleic Acid Therapeutics.2022 March, 32(3), 206–220.
720008206ZH,2024年1月