使用沃特世串联四极杆质谱仪上的全扫描谱MS/MS功能检测和表征生物体液中的药物代谢物
摘要
快速筛查生物体液样品中的药物代谢物,能帮助研究人员识别代谢软点,检测具有潜在毒性的代谢物,并改善候选药物的药代动力学特征。这一过程可能复杂又耗时,需要采集并分析MS和MS/MS数据。串联四极杆质谱仪在MRM模式下具有出色的灵敏度,因此广泛用于药物浓度测定,除此之外,这类质谱仪还具备其他功能,可应用于药物代谢表征研究。沃特世串联四极杆质谱仪的“全扫描谱”采集模式可利用特征碎片离子和恒定中性丢失快速检测和表征药物的生物转化过程。本文所述实验利用“全扫描谱”和LC-MS/MS方法分析了尿液中的美沙吡啉代谢物。“全扫描谱”模式结合母离子监测,通过监测给药化合物的多个共有碎片离子,帮助定位代谢位点,检出了30多种药物相关代谢物。
优势
- 无偏差的数据依赖型采集
- 简单易用的MS/MS功能
- 基于共有碎片离子或恒定中性丢失进行特征检测
- 单次分析即可采集母离子和子离子
简介
从ADME分析、体外筛查到体内毒代动力学监测研究,药物代谢物的检测和表征在药物发现和开发中发挥着关键作用1。从这些研究中获得的信息可用于通过体外筛查鉴定代谢软点,在早期动物研究中确定代谢途径和速率,以及比较不同剂量组、性别和物种之间的代谢特征,帮助拓宽毒理学研究的覆盖范围2。
液-质联用技术具有出色的灵敏度和选择性,有助于快速方法开发,能提供信息丰富的质谱数据,且能兼容生物样品,已成为DMPK研究的首选平台。串联四极杆质谱仪广泛应用于生物分析实验室,可提供高灵敏度的定量数据,帮助测量候选药物的药物暴露量并确定药代动力学(PK)参数3。除了需要生成PK信息,还需要监测和分析生物体液中药物在生物转化过程中的变化。这样可确保在安全性评估研究的代谢分析中具有足够的覆盖范围、监测不同物种和剂量水平之间代谢物相对丰度的变化以及检测具有潜在毒性的代谢物。这款串联四极杆质谱仪采用特殊设计,方便在MS与MS/MS模式之间快速切换,从而能够在LC窄峰的时间范围内采集到高质量的碎片离子谱图。“全扫描谱”采集已应用于基于代谢结合物(如葡糖苷酸或谷胱甘肽)的特征共有碎片离子或恒定中性丢失,高灵敏度分析生物体液中药物相关的生物转化过程。
实验
样品描述
对雄性Wistar大鼠重复口服给予美沙吡林(图1)后收集尿样4。 分别在给药第2、4和6天的24小时内采集样品。有关动物研究和样品前处理的完整信息,请参阅沃特世应用纪要720008016ZH5。 对照Wistar大鼠尿液购自BioIVT(美国纽约州)。将50 μL尿液与200 μL冰乙腈混合,制得生物体液样品,将样品涡旋混合,然后在-20 °C下储存1 h。将制得的样品在9000 g转速下离心5 min,并将上清液转移至全回收样品瓶中进行LC-MS/MS分析。
方法条件
完成样品提取后,取2 μL样品上样至2.1 x 100 mm Cortecs™ C18 2.7 µm色谱柱。色谱柱柱温保持在40 °C,使用0.1%甲酸的水溶液作为流动相A,含0.1%甲酸的95:5 (v/v)乙腈:水溶液作为流动相B,在10分钟内以线性反相梯度,在600 μL/min的流速下洗脱(表1)。 使用正离子ESI质谱,在“全扫描谱”模式下采用母离子扫描或恒定中性丢失触发采集(如表2所示),监测色谱柱洗脱液。
液相色谱条件
|
液相色谱系统: |
ACQUITY™ I Class UPLC™ |
|
检测器: |
Xevo™ TQ-XS |
|
样品瓶: |
沃特世全回收样品瓶(P/N:186004631) |
|
色谱柱: |
CORTECS Premier T3色谱柱;2.7 µm, 2.1 × 100 mm(P/N:186010473) |
|
柱温: |
40 °C |
|
样品温度: |
8 °C |
|
进样体积: |
2 µL(尿液) |
|
流速: |
600 µL/min |
|
流动相A: |
0.1 %(v/v)甲酸水溶液 |
|
流动相B: |
含0.1%甲酸(v/v)的95%乙腈:5%水溶液 |
|
梯度: |
参见梯度表 |
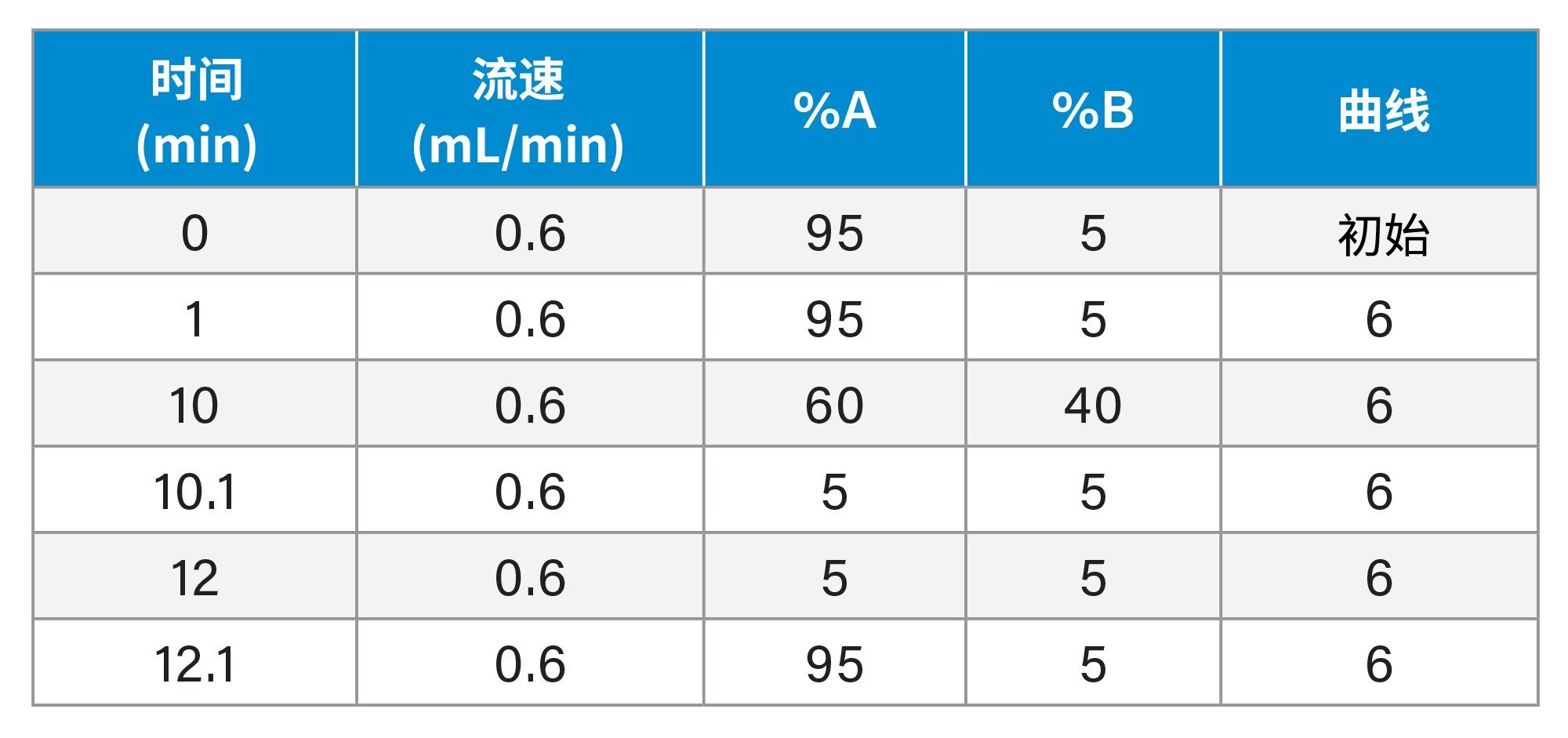
表2.质谱条件
|
质谱系统: |
Xevo TQ-XS |
|
电离模式: |
正离子 |
|
采集范围: |
ESI |
|
毛细管电压: |
2.0 kV |
|
碰撞能量: |
30 eV |
|
锥孔电压: |
30 V |
|
采集: |
全扫描谱,使用m/z=97.1、119.2、133.2的母离子或恒定中性丢失80.1和176.1 |
数据管理
|
色谱软件: |
MassLynx™ v4.2 |
|
质谱软件: |
MassLynxv4.2 |
|
信息学软件: |
MassLynx v4.2 |
*注5. 指定每种软件的版本。
结果与讨论
利用LC-MS/MS鉴定生物体液中的代谢物时,首先需要检测尿液和血浆等基质中的药物相关物质,然后采集母离子和子离子谱图数据进行分析。随后再基于给药化合物的母离子质量数和碎裂模式、所检出代谢物的母离子和子离子谱图以及已知的代谢转化(官能化和偶联)合理解释这些数据。某一分析物要被接受为药物相关代谢物,必须满足以下标准:6
- 代谢物的产生有合理的生物转化解释
- 代谢物与母体化合物至少共有一种碎片离子,或至少共有一种中性丢失
- 该分析物在对照品或给药前样品中未检出,并且与母体化合物相比,必须在合理的保留时间范围内洗脱
- 所有在溶剂前沿洗脱的组分均应排除,避免假阳性
“全扫描谱”采集利用沃特世串联四极杆质谱仪离子光学元件的灵活性,使用各种MS(MS)采集模式(例如恒定中性丢失(CNL)或共有碎片离子)筛查药物相关分析物。检测到这些特征(强度高于用户指定的阈值)时,仪器将自动切换模式,为所检测特征的基峰采集靶向MS/MS数据。这种数据依赖型采集模式(DDA)为代谢物筛查提供了一种高灵敏度、高选择性的模式,有利于随后进行靶向MS/MS数据采集,从而获得背景噪音更低的高质量MS谱图。
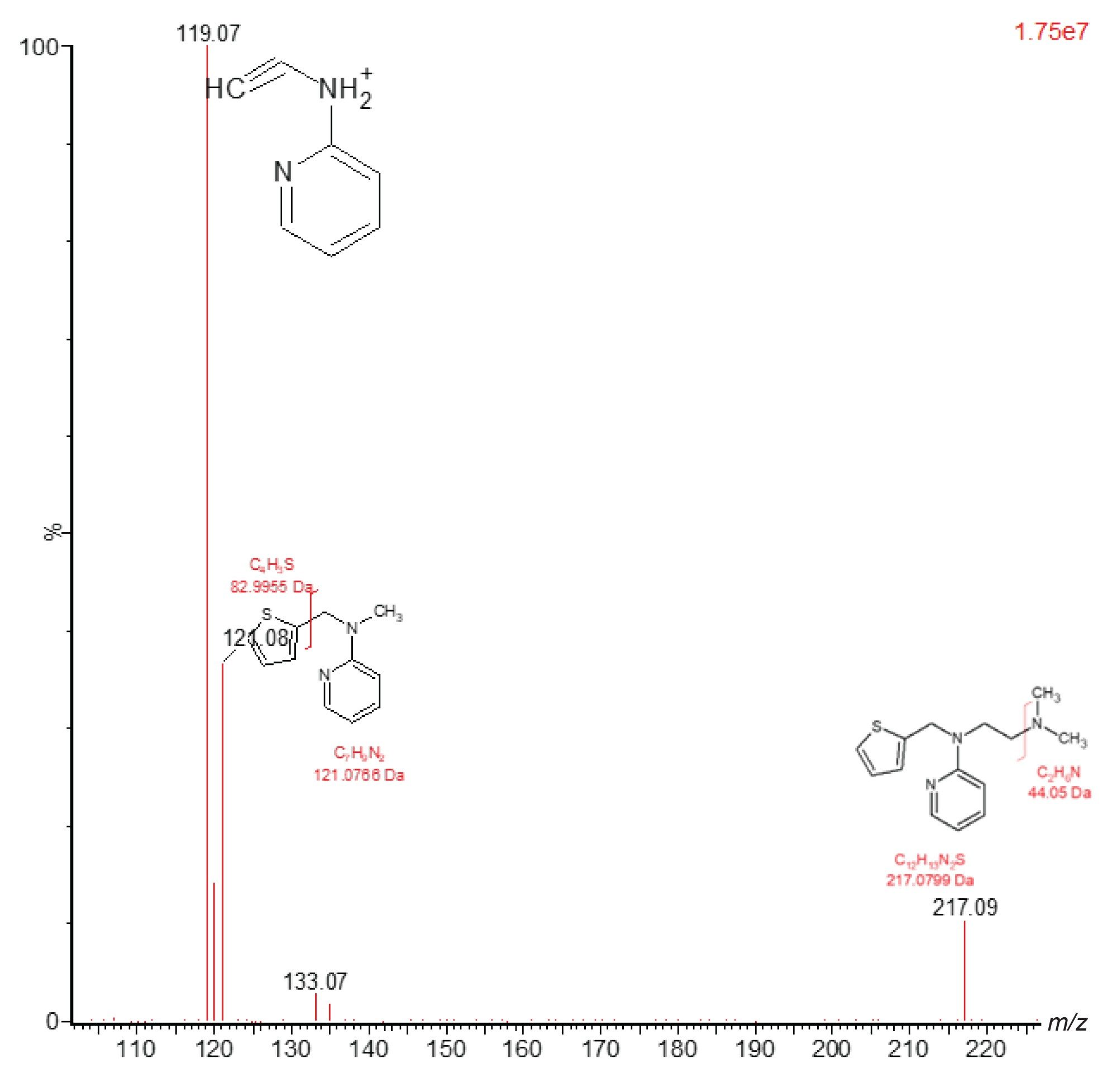
为了说明“全扫描谱”采集在药物代谢物筛查和表征中的应用,我们分析了大鼠口服抗组胺药和抗胆碱能药物美沙吡啉后的尿样。美沙吡啉的化学式为C14H19N3S,对美沙吡啉确证标准品(m/z=262.23)进行正离子MS/MS分析得到了特征碎片离子m/z=96.88、119.17、121.17、133.07和217.09。这些碎片离子可合理解释为:噻吩环碎片离子(m/z=96.88)、噻吩环、脂肪链以及吡啶环上的叔胺基团断裂(m/z=119.17)、噻吩环和脂肪链断裂留下叔胺和吡啶基团(m/z=121.17)、噻吩环和叔胺断裂留下吡啶环和脂肪链(m/z=133.07),最后是叔胺断裂(m/z=217.09),图2。
母离子扫描采集
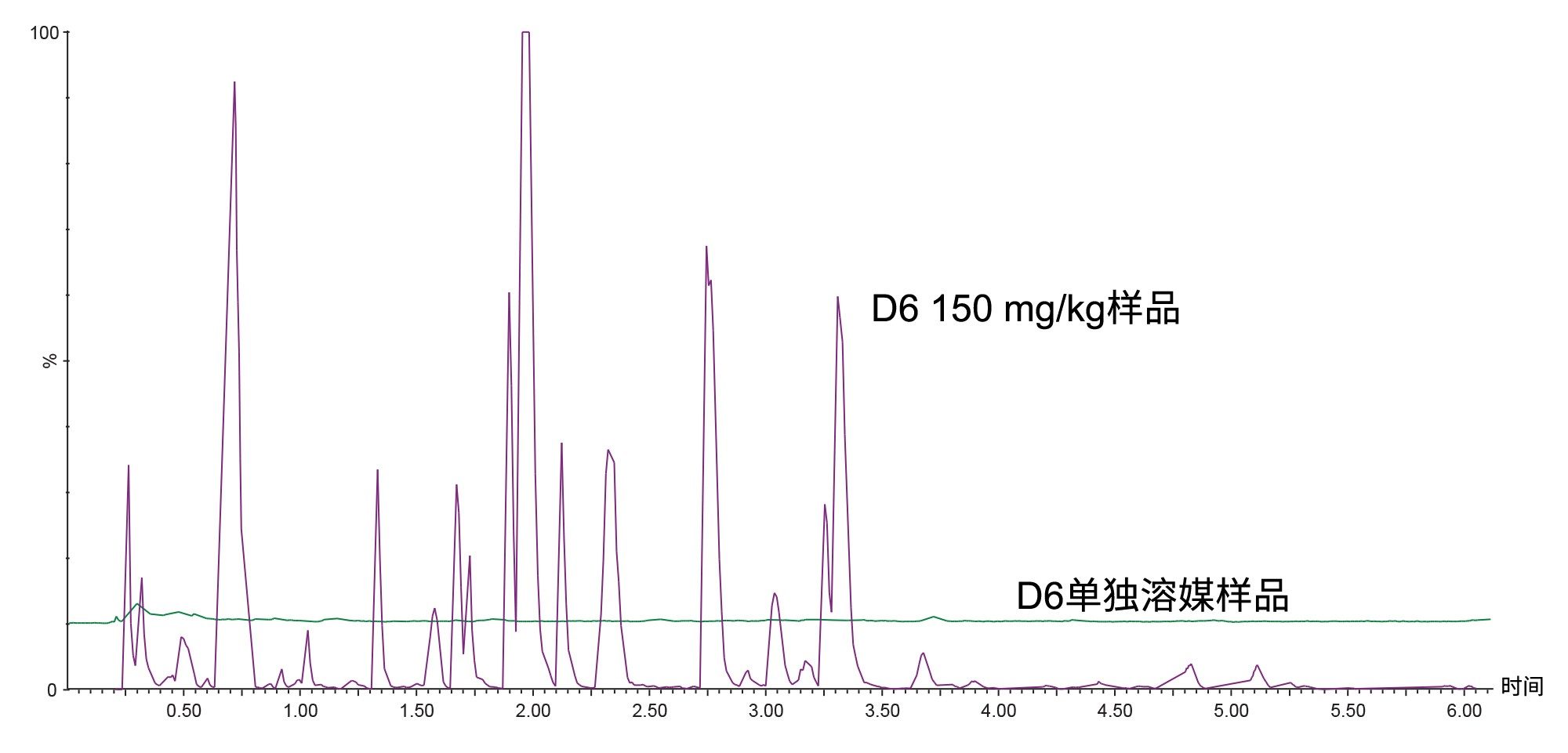
在“全扫描谱”模式下,使用母离子扫描m/z=96.88、121.17和137.20(m/z=137.20表示121.17的羟基化部分),在m/z=50–600的质量范围内采集尿液的母离子MS/MS数据。使用质心模式采集数据,扫描时间为0.5 s,碰撞能量为30 eV,之后切换到MS/MS模式,扫描时间为0.2 s。当信号强度降至1,000计数以下时,采集作业返回母离子扫描模式。使用m/z=96.88的母离子分析单独溶媒样品和D6 150 mg/kg尿液样品的数据如图3所示。数据表明,使用母离子m/z=96.88的“全扫描谱”采集在给药样品中检测到多个峰,而这些峰在单独溶媒样品中未检出。此外,单独溶媒样品的叠加迹线未显示任何药物相关物质的迹象,表明该采集过程具有选择性。图4所示的数据比较了分别使用m/z=96.88、121.17和137.20这三种母离子分析同一D6 150 mg/kg尿液样品获得的TIC色谱图。从该数据可以看出,某些分析物在使用上述三个母离子质量数时均检出,例如,tR=1.35 min处的峰,而大多数峰仅在使用m/z=96.88、121.17采集时检出。这表明了该采集模式的选择性。不对称峰形是DDA采集过程中产生的伪影。
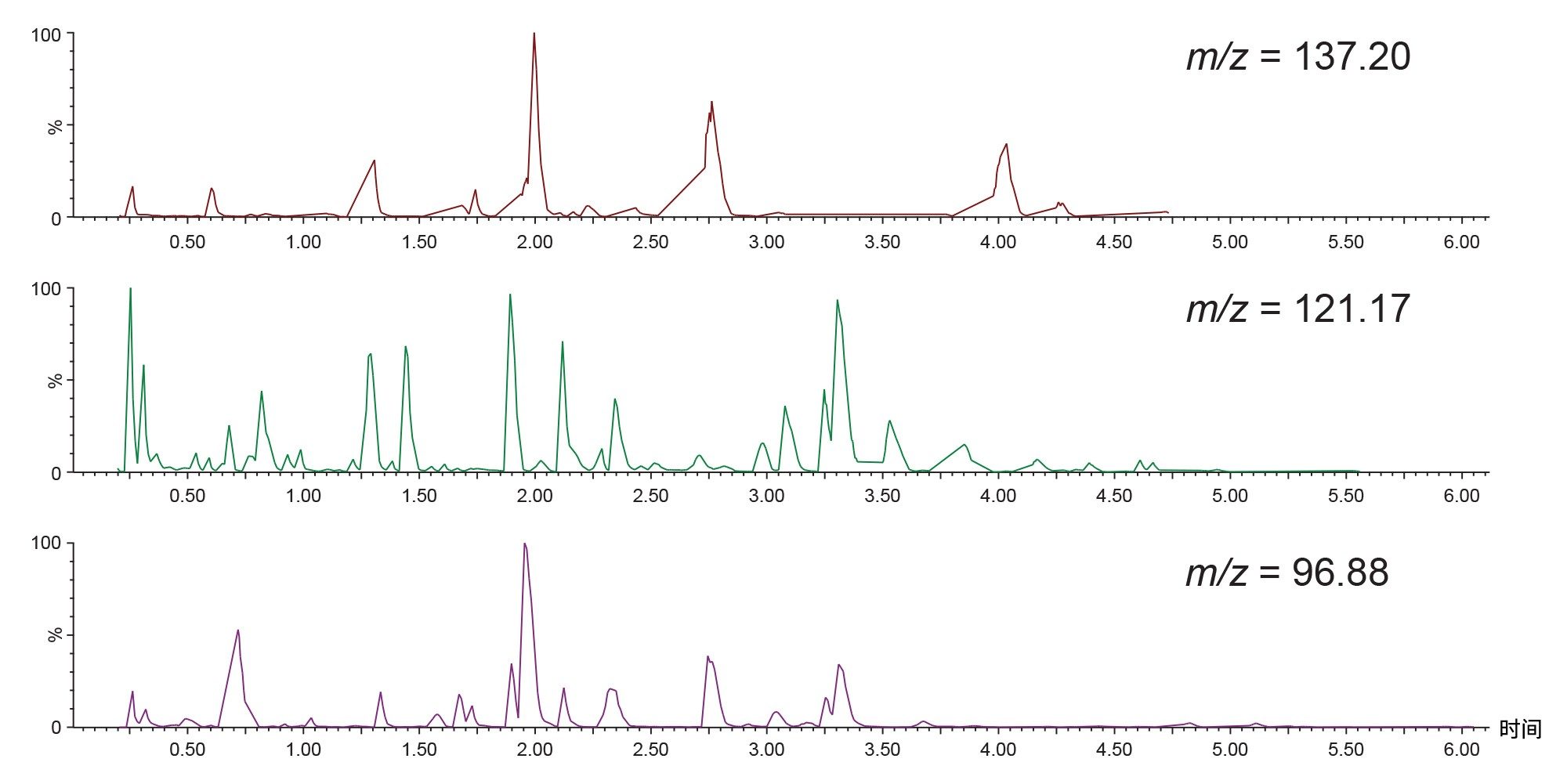
“全扫描谱”是一种DDA采集模式,利用扫描采集(在本例中为母离子)在单次分析中同时采集MS和MS/MS谱图数据。得到的MS和MS/MS谱图用于代谢物分类和表征。使用这种分析模式共检出34种药物相关代谢物。下面的图5显示了使用m/z=96.88的母离子采集到的MS和MS/MS谱图示例。所示数据展示了美沙吡啉代谢物:N-氧化物(tR=3.3 min)、羟基化(tR=3.0 min)和双羟基化(tR=2.7 min)的MS和MS/MS谱图。值得注意的是,由于DDA采集的特异性,所生成的MS/MS谱图不存在无关的谱图噪音,因此更易于解析。
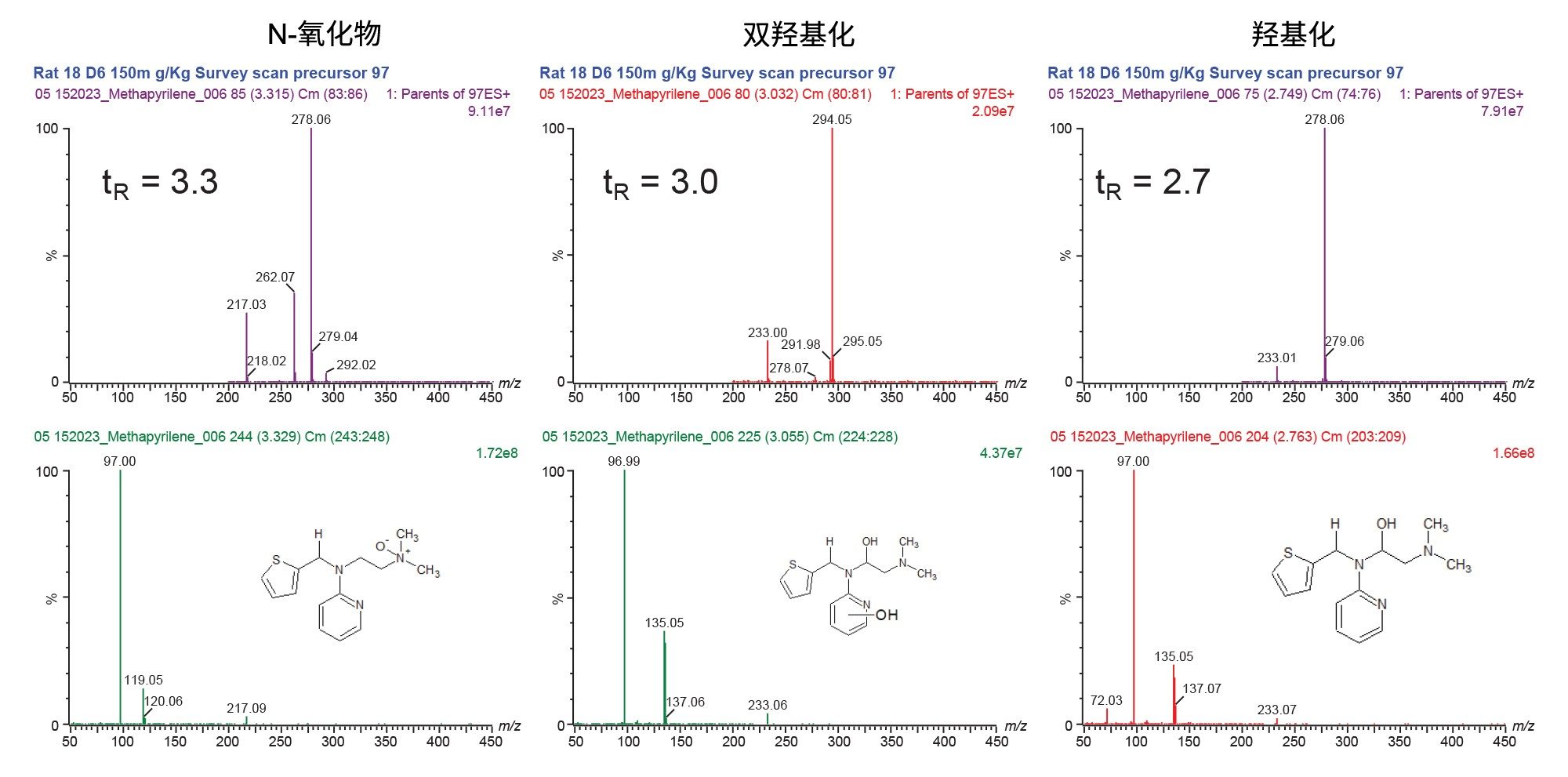
图6所示的数据展示了使用母离子m/z=121.17的“全扫描谱”采集获得的MS和MS/MS谱图。示例数据显示了美沙吡啉(给药化合物)及其代谢物N-氧化物(tR=3.3 min)和N-O-葡糖苷酸(tR=1.8 min)的谱图。与如图5所示数据一样,MS/MS谱图非常清晰,不存在背景噪音,简化了结构表征过程。沃特世串联四极杆质谱仪的快速采集功能可在一次分析运行中扫描多个母离子,由此实现快速、全面的代谢物检测和代谢位点定位。
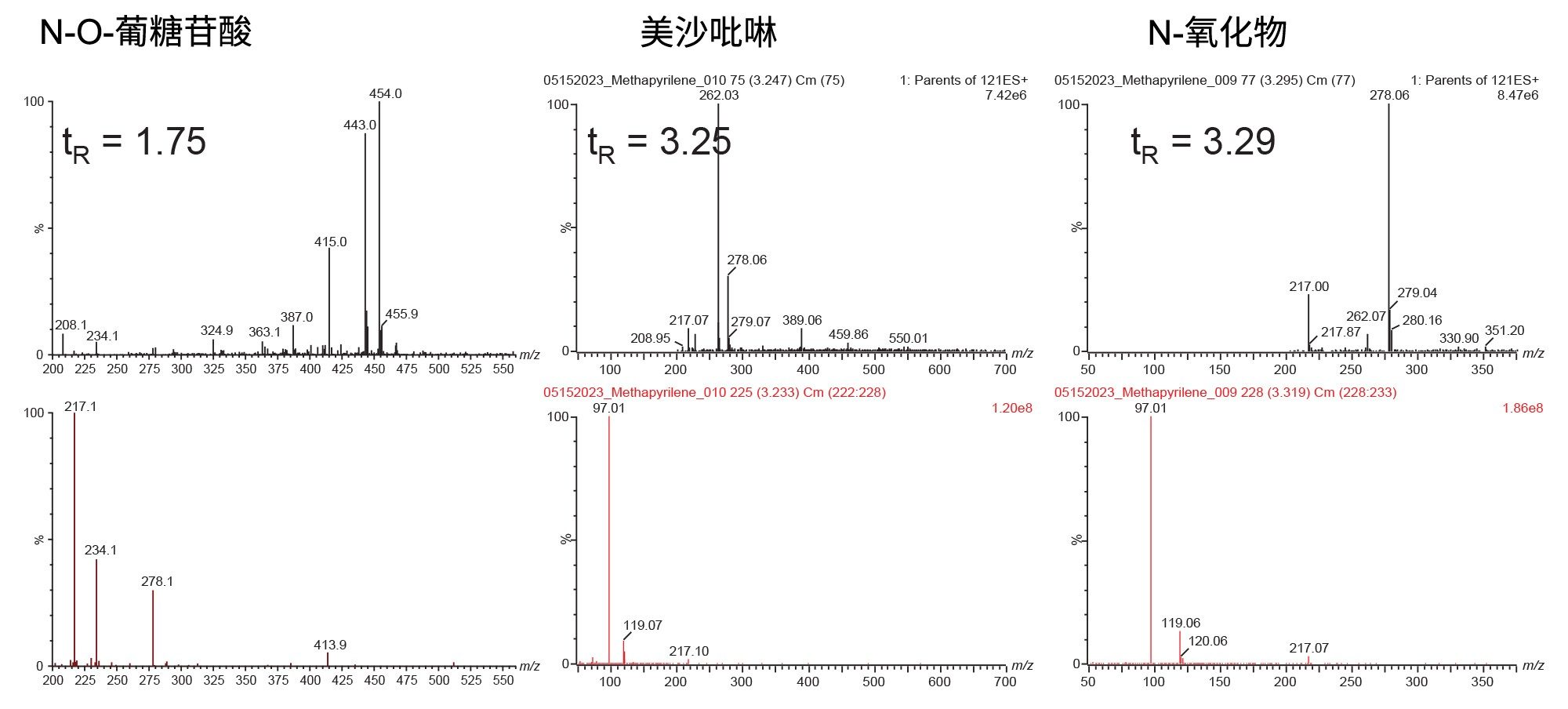
恒定中性丢失(CNL)也是一种MS/MS数据采集模式,根据丢失的中性碎片离子来检测化合物。这种采集模式常用于筛查与极性部分(如硫酸盐、葡萄糖醛酸和谷胱甘肽)偶联形成的药物代谢物。为了说明这种采集模式,我们使用中性丢失为176.12 Da的“全扫描谱”在正离子ESI模式下分析了美沙吡啉尿液样品,监测葡糖苷酸代谢物(采集参数与母离子扫描模式下的参数类似)。图7展示了使用D6单独溶媒和D6 150 mg/kg样品获得的数据。从该数据可以看出,在单独溶媒样品中检出多个峰显示葡糖苷酸结合物(176.12 Da)的丢失信号,它们很可能是内源性化合物(例如,食品和环境)的结合物。与单独溶媒样品相比,D6 150 mg/kg样品分析显示葡糖苷酸结合物显著更多。
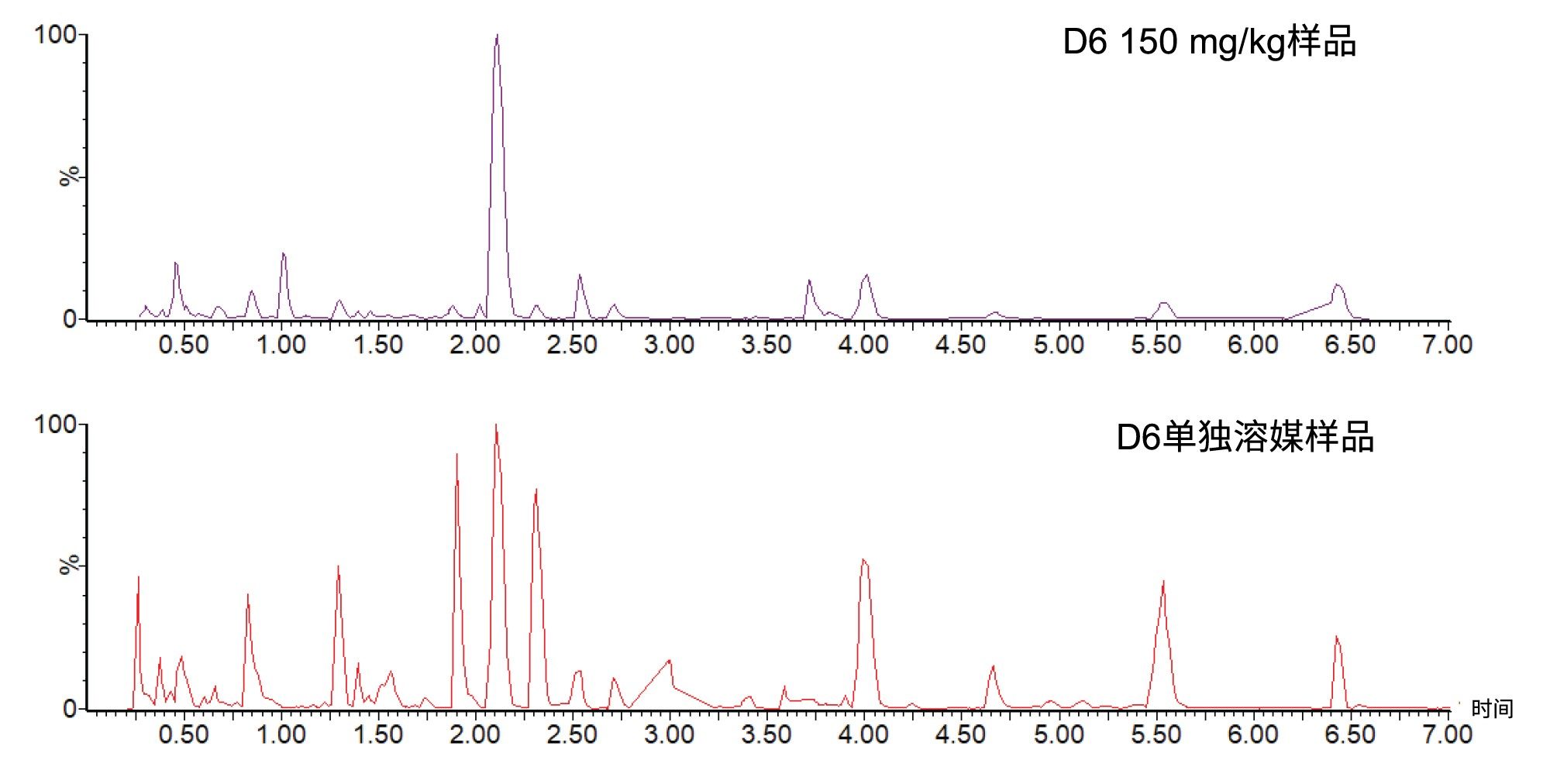
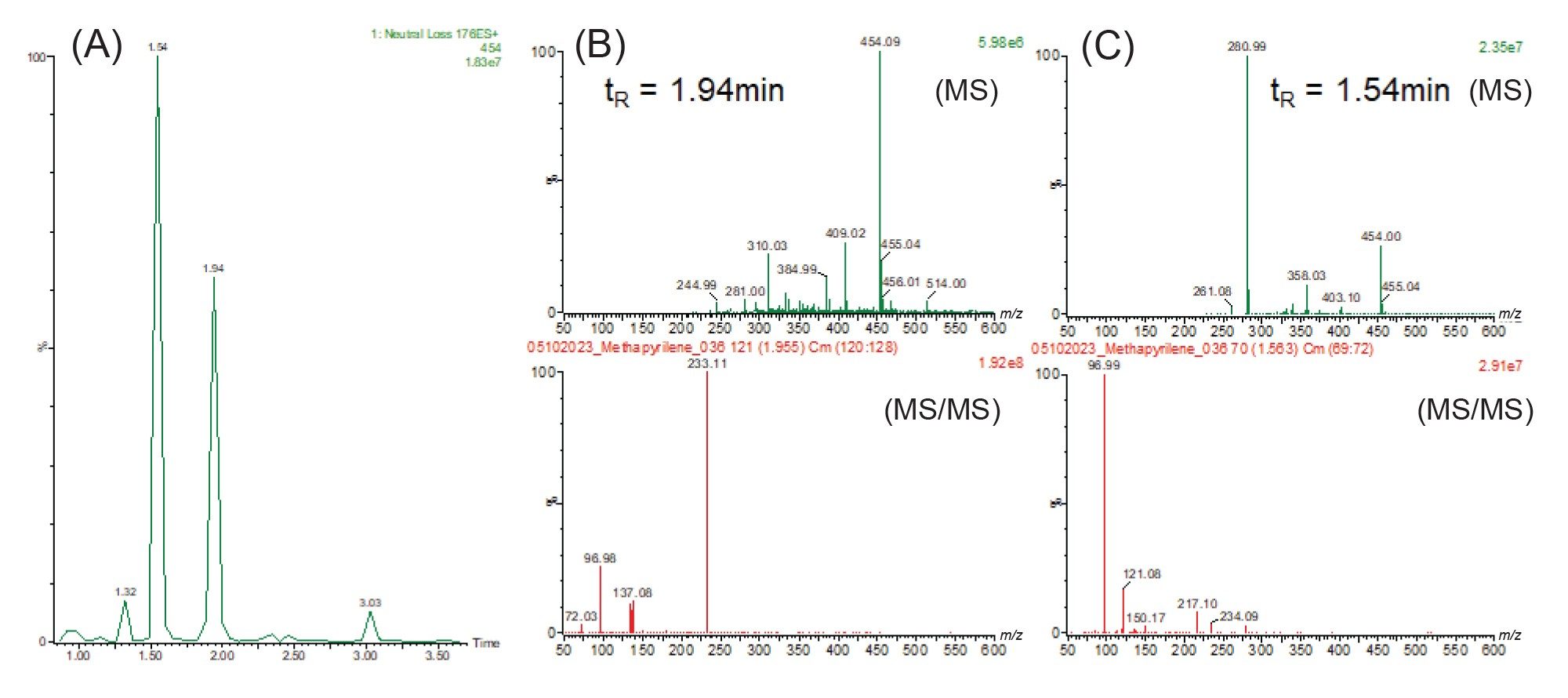
对接受美沙吡啉给药的动物的尿液进行CNL葡糖苷酸(-176 DA)分析,进一步分析是否存在药物相关的葡糖苷酸代谢物。结果表明,存在几种由美沙吡啉经过多种官能化作用产生的药物相关葡糖苷酸结合物,包括O-葡糖苷酸、N-O-葡糖苷酸、去甲基O-葡糖苷酸和二羟基葡糖苷酸。图8中的数据显示了美沙吡啉O-葡糖苷酸代谢物(m/z=454.1)的提取离子流色谱图(A)。数据显示存在四种O-葡糖苷酸代谢物。tR=1.94和1.54 min处两个峰得到的MS和MS-MS谱图如图8B和C所示。tR=1.94 min处峰的MS谱图(图8B)显示了MS基峰m/z=454.1和MS/MS碎片离子m/z=233.1、137.08和96.88,该代谢物可以合理解释为吡啶环羟基化所形成代谢物的葡糖苷酸结合物。而tR=1.54处峰得到的MS/MS碎片离子(图8C)与母体化合物美沙吡啉(m/z=217.10、121.08和96.99)一致,表明其为N-氧化物代谢物的葡糖苷酸结合物。
结论
药物代谢物的检测和表征在药物发现和开发过程中发挥着至关重要的作用。沃特世串联四极杆质谱仪采用新型碰撞室设计,可在不同的采集模式之间快速切换。“全扫描谱”正是利用此功能,通过共有碎片离子或恒定中性丢失选择性地筛查药物相关物质。该采集模式用于研究大鼠口服给予美沙吡啉后尿液中的药物代谢物。“全扫描谱”采集模式提供了一种快速、灵敏且特异性的数据分析模式,可以生成清晰的MS/MS谱图,简化结构解析。使用该方法获得的靶向MS/MS谱图有助于快速、简单地表征药物代谢物。本研究使用该方法共检测并表征了尿液中的30多种药物相关代谢物。使用这种采集模式检出了之前未报告的美沙吡啉代谢物,例如N-O-葡糖苷酸。
参考资料
- Molloy BJ, King A, Mullin LG, Gethings LA, Riley R, Plumb RS, Wilson ID.Rapid Determination of the Pharmacokinetics and Metabolic Fate of Gefitinib in the Mouse Using a Combination of UPLC/MS/MS, UPLC/QToF/MS, and Ion Mobility (IM)-Enabled UPLC/QToF/MS.Xenobiotica.2021 Apr;51(4):434–446.doi: 10.1080/00498254.2020.1859643.
- lanz J, Williams G, Dayer J, Délémonté T, Gertsch W, Ramstein P, Aichholz R, Trunzer M, Pearson D. Evaluation of Relative MS Response Factors of Drug Metabolites for Semi-Quantitative Assessment of Chemical Liabilities in Drug Discovery.J Mass Spectrom.2017 Apr;52(4):210–217.doi: 10.1002/jms.3918. PMID: 28152561.
- Ackermann BL, Berna MJ, Murphy AT.Recent Advances in Use of LC/MS/MS for Quantitative High-Throughput Bioanalytical Support of Drug Discovery.Curr Top Med Chem.2002 Jan;2(1):53–66.doi: 10.2174/1568026023394605.
- Geenen S, Guallar-Hoyas C, Michopoulos F, Kenna JG, Kolaja KL, Westerhoff HV, Thomas P, Wilson ID.HPLC-MS/MS Methods for the Quantitative Analysis of 5-Oxoproline (Pyroglutamate) in Rat Plasma and Hepatic Cell Line Culture Medium. J Pharm Biomed Anal. 2011 Nov 1;56(3):655–63.doi: 10.1016/j.jpba.2011.06.001.
- “DMPK研究中的串联四极杆采集模式”, 沃特世应用纪要 720008016ZH.
- Molloy BJ, King A, Gethings LA, Plumb RS, Mortishire-Smith RJ, Wilson ID.Investigation of the Pharmacokinetics and Metabolic Fate of Fasiglifam (Tak-875) in Male and Female Rats Following Oral and Intravenous Administration.Xenobiotica.2023 Feb;53(2):93-105.doi: 10.1080/00498254.2023.2179952.
720008228ZH,2024年1月