使用IntelliStart™和RADAR技术开发和监测高灵敏度生物分析MRM方法
摘要
高灵敏度生物分析方法被广泛应用于药物发现和开发的整个过程,旨在提供准确的定量数据,为DMPK、毒代动力学(TK)研究和随机临床试验提供支持。过去25年来,串联四极杆LC-MS/MS已成为定量生物分析的首选技术。开发符合用户需求的可靠方法,需要仔细评估LC和MS采集参数。沃特世串联四极杆质谱仪系统配备IntelliStart软件,该软件支持全自动开发稳定、高灵敏度的MRM方法。IntelliStart可优化电离极性、母离子、子离子、离子源电压和碰撞能量,确定理想的采集参数。Xevo™串联质谱仪还配备RADAR技术,可同时监测LC背景信号,简化方法开发和分析监测。
优势
- 用于生物分析研究的LC-MS/MS方法开发
- 使用IntelliStart技术自动优化MRM条件
- 快速、高效地开发理想的SIR和MRM条件,非专家和专家用户均适用
- 使用RADAR技术监测背景信号,以简化LC/MS方法开发、确保方法适用性和故障诊断排除
简介
多重反应监测(MRM)与液相色谱法相结合的串联四极杆质谱分析法,由于具有出色的特异性、选择性和灵敏度,已成为高灵敏度定量检测生物体液中候选药物的首选技术1。开发快速、高灵敏度,同时保持稳定、可靠性和可转移性的定量生物分析方法通常具有挑战性。这些方法需要确定理想的MS离子源条件、操作极性、母离子、子离子和碰撞能量,还需要开发快速、可靠的色谱条件。开发这些LC-MS/MS方法通常很耗时,并且过去通常由专家用户来开发。
优化LC分离方法通常需要监测背景离子,以尽量减少基质中分析物的干扰,同时尽可能提高样品通量。随着药物开发研究进展到随机临床试验阶段,样品基质会因为年龄、生活方式、健康状况、饮食以及是否同时服用药物等方面的变化而变得更加复杂2。在采集定量MRM信号的同时监测色谱背景信号,简化了监测这些内源性和外源性化合物对分析性能影响的方法。
本文介绍了Xevo串联四极杆质谱仪与IntelliStart软件结合用于快速开发灵敏、稳定的LC-MS/MS生物分析方法,以及利用RADAR技术同时监测背景基质离子。
实验
样品描述
为了阐明IntelliStart软件和RADAR技术的应用,我们开发了一种定量分析大鼠血浆和尿液中美沙吡啉的生物分析方法。有关动物研究和样品前处理的完整信息,请参阅沃特世应用纪要“DMPK研究中的串联四极杆采集模式”,720008016ZH3。对照wistar大鼠血浆和尿液均购自BioIVT(美国纽约州)。
取2 μL萃取样品进样至2.1 × 50 mm CORTECS™ C8 2.7 µm色谱柱,用于分析血浆和尿液样品。色谱柱柱温保持在40 °C,使用0.1%甲酸水溶液作为流动相溶剂A,含0.1%甲酸的95:5 (v/v)乙腈:水溶液作为流动相B,在2.5分钟内以线性反相梯度,在600 μL/min的流速下洗脱(表1)。色谱柱洗脱液采用正离子ESi质谱在MRM模式下进行监测。色谱柱洗脱液采用正离子ESi质谱在MRM模式下进行监测,通道m/z = 262.2→119.2,锥孔电压为30 V,碰撞能量为20 eV(表2)。
液相色谱条件
|
液相色谱系统: |
ACQUITY™ I Class UPLC™ |
|
检测: |
Xevo TQ-XS |
|
样品瓶: |
沃特世全回收样品瓶,(P/N:186004631) |
|
色谱柱: |
CORTECS Premier T3色谱柱;2.7 µm, 2.1 × 100 mm(P/N:186010473) |
|
柱温: |
40 °C |
|
样品温度: |
8 °C |
|
进样体积: |
2 µL(尿液),1 µL(血浆) |
|
流速: |
600 µL/min |
|
流动相A: |
0.1 %(v/v)甲酸水溶液 |
|
流动相B: |
含0.1%甲酸(v/v)的95%乙腈:5%水溶液 |
|
梯度: |
参见梯度表,表1 |
表1
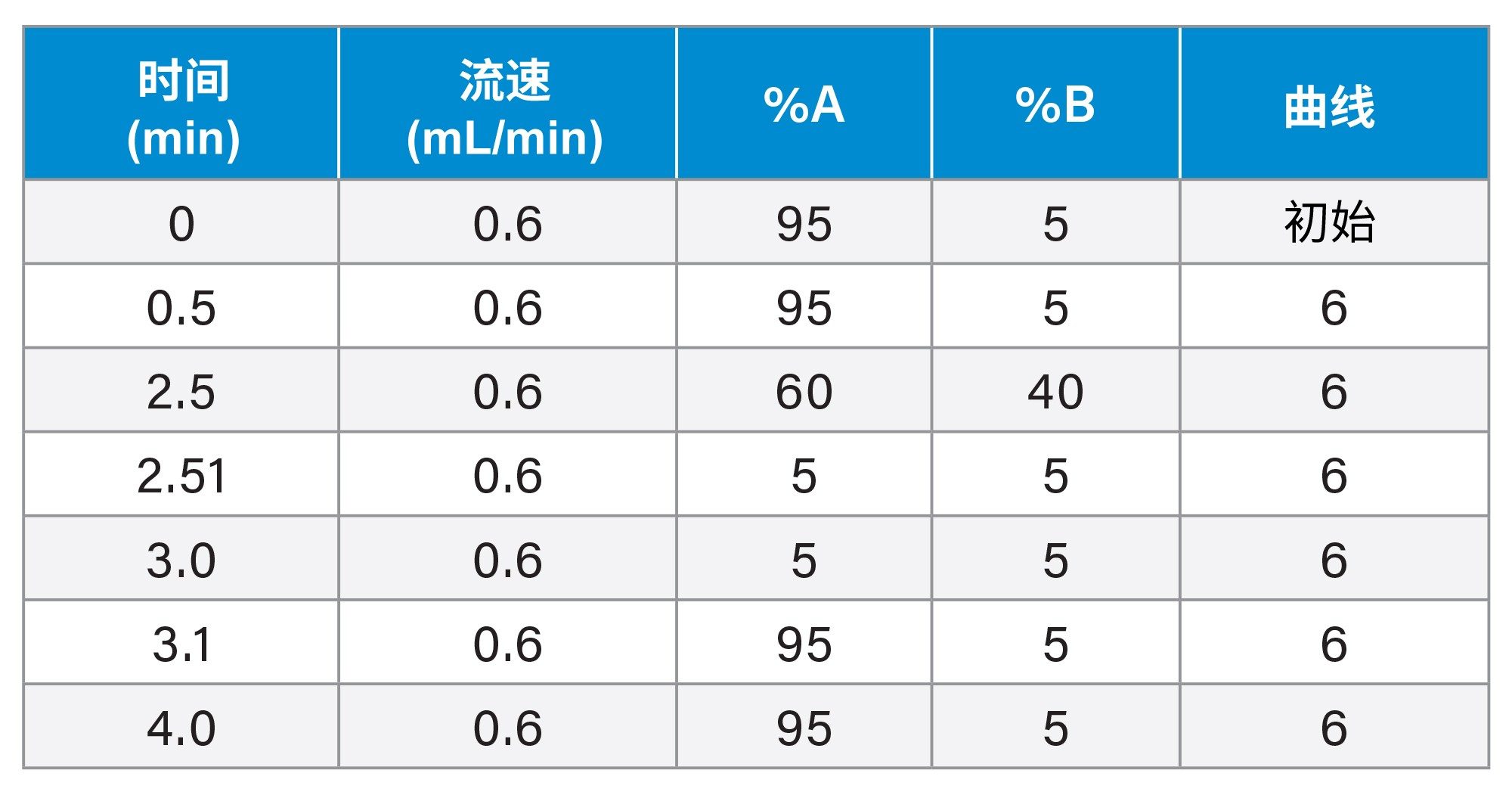
质谱条件
|
质谱系统: |
Xevo TQ-XS |
|
电离模式: |
正离子ESi |
|
采集范围: |
100~800 m/z(RADAR采集) |
|
毛细管电压: |
2.0 kV |
|
碰撞能量: |
20 eV |
|
锥孔电压: |
30 V |
|
MRM通道: |
m/z=262.2→119.2 |
数据管理
|
色谱软件: |
MassLynx™ v4.2 |
|
质谱软件: |
MassLynxv4.2 |
|
信息学软件: |
TargetLynx™ v4.2 |
结果与讨论
多重反应监测是利用质谱仪对复杂混合物进行痕量测量最灵敏的分析模式。在这种操作模式下,第一个分离四极杆设置为仅允许特定单个(或多个)离子(m/z值)通过。选定的离子在碰撞室中碎裂,并被引导至最终的分辨四极杆,该四极杆经过设置,仅允许选定的碎片离子通过,从而提供高选择性和高特异性的分析方法。这种特异性和选择性可显著降低背景“噪音”,从而实现高灵敏度分析,尤其是与高分离度色谱联用时。因此,基于MRM的LC-MS/MS已成为高灵敏度定量生物体液中药物及其代谢物的首选技术。
为了展示MRM分析在定量口服美沙吡啉(一种抗组胺药和抗胆碱能药,图1)的血浆样品中药物化合物的发展和应用,本研究对雄性Wistar大鼠按150 mg/kg的剂量口服美沙吡啉进行了反相UPLC-MS/MS分析4。
将100 ng/mL(溶于50:50甲醇:水溶液(0.1%甲酸))美沙吡啉溶液以5 μL/min的速率通过机载流路注入Xevo TQ-XS质谱仪。脱溶剂气温度为300 °C,脱溶剂气体(氮气)流速为500 L/h。向IntelliStart软件输入的原始数据为美沙吡啉元素组成(C14H19N3S),并在2~100 V的锥孔电压范围和2~80 eV的碰撞能量范围内进行了条件优化(图2)。将碎片离子质量数下限设置为m/z=100。在正离子和负离子模式下评估信号响应。根据所得结果,灵敏度和特异性最高的参数为正离子通道m/z = 262.2→119.2,碰撞能量为20 eV,锥孔电压为48 V。TQ-XS的锥孔电压曲线在15~50 V之间基本平坦,因此在分析中采用了30 V的锥孔电压(图2)。
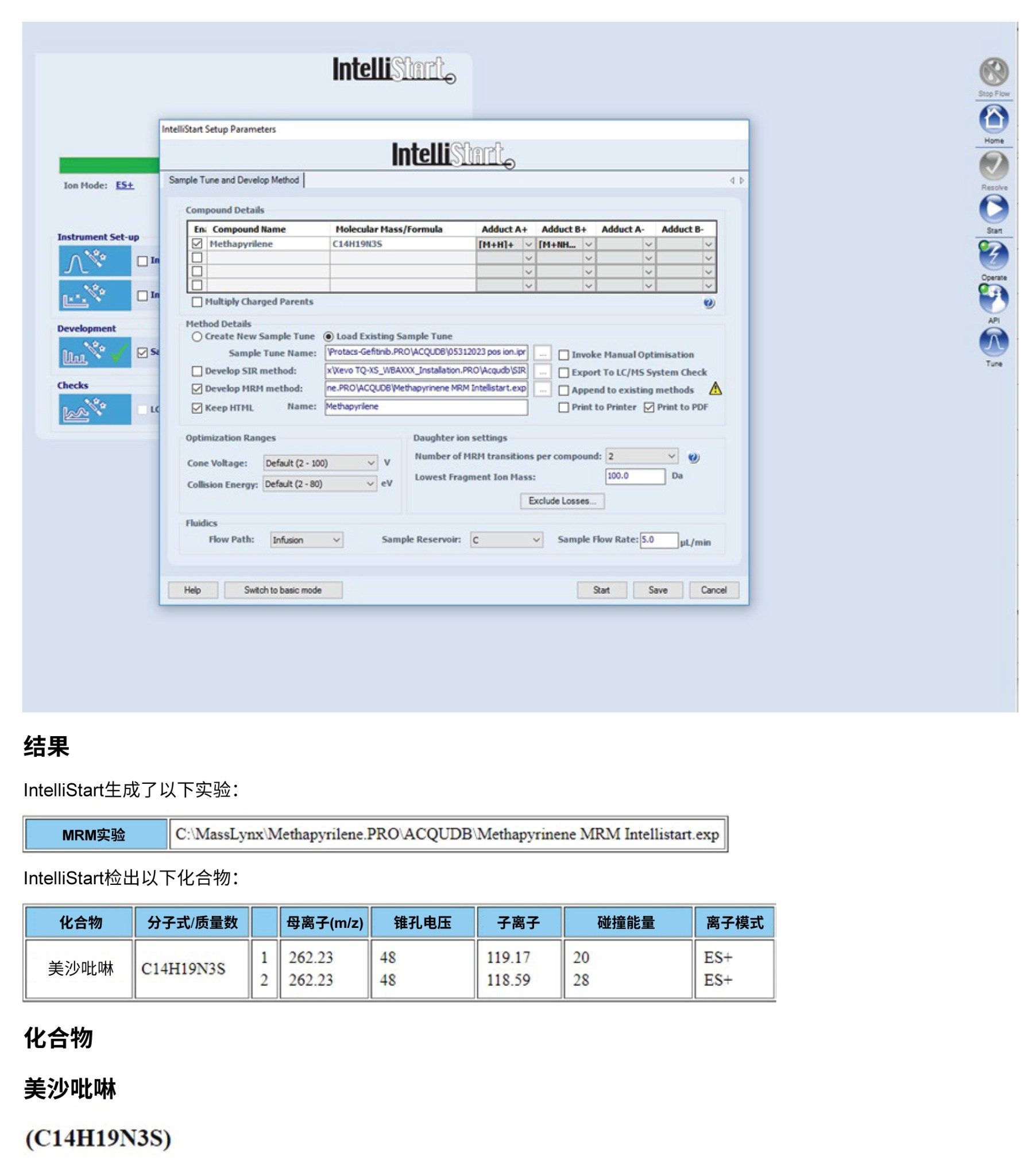
IntelliStart选择碎片离子m/z=119.17作为灵敏度最高的子离子。下面图3中的数据展示了碰撞能量30 eV、正离子模式下美沙吡啉(m/z=262.2)的碎片离子谱图。
美沙吡啉分子的碎裂产生了三种主要离子:m/z = 217.09、121.08和119.07,其中m/z = 119.2的强度最高,验证了IntelliStart碎片离子优化。该离子可以解释为美沙吡啉分子失去了噻吩环和脂肪族叔胺链。
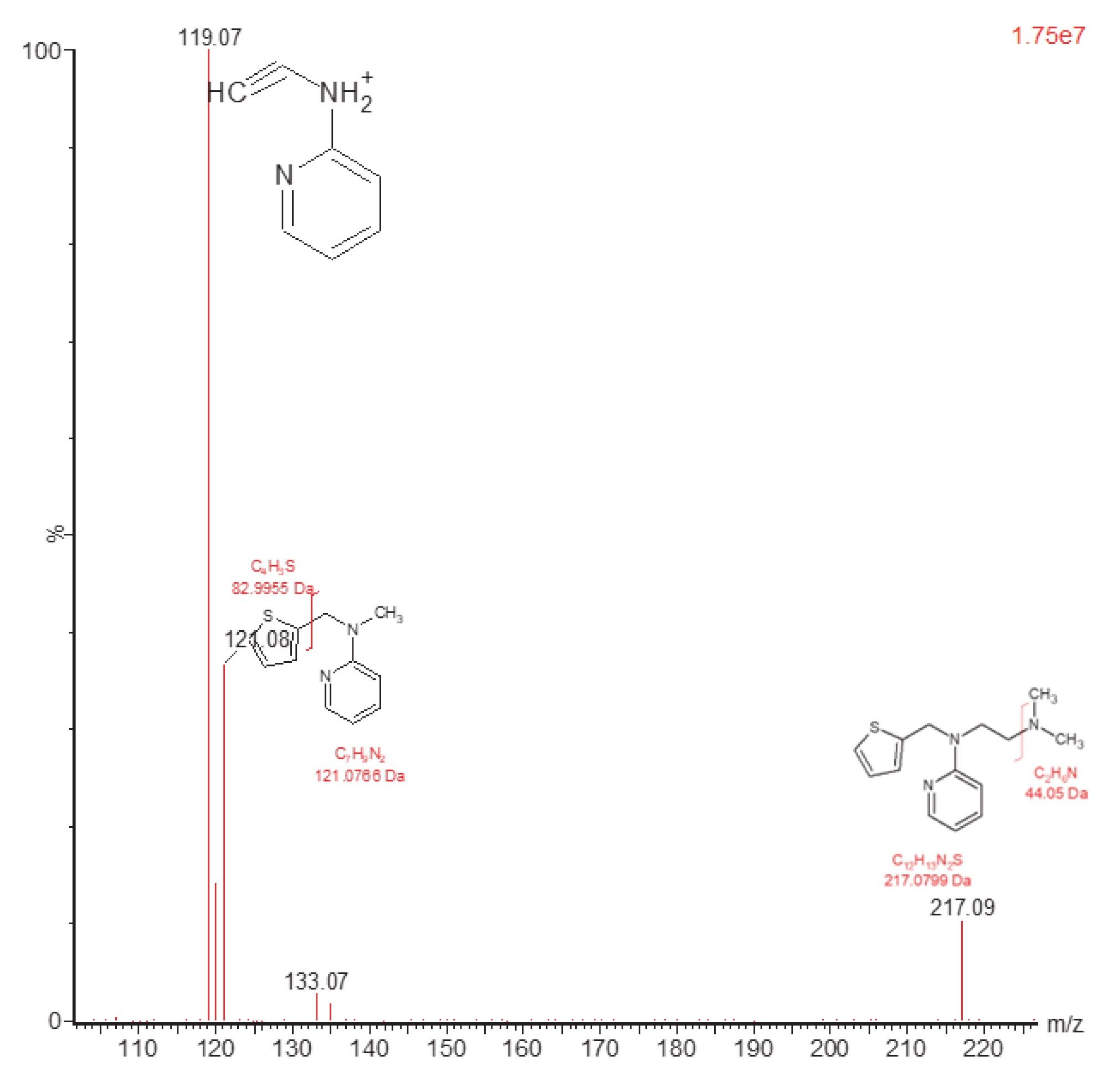
IntelliStart生成的优化参数表明,在20 eV的碰撞能量下可产生最灵敏的通道(262.2→119.2)。美沙吡啉使用反相梯度色谱分离(分析时间10分钟)和5~50 eV的碰撞能量范围,通过手动评估峰响应来确认碰撞能量的优化结果(图4)。
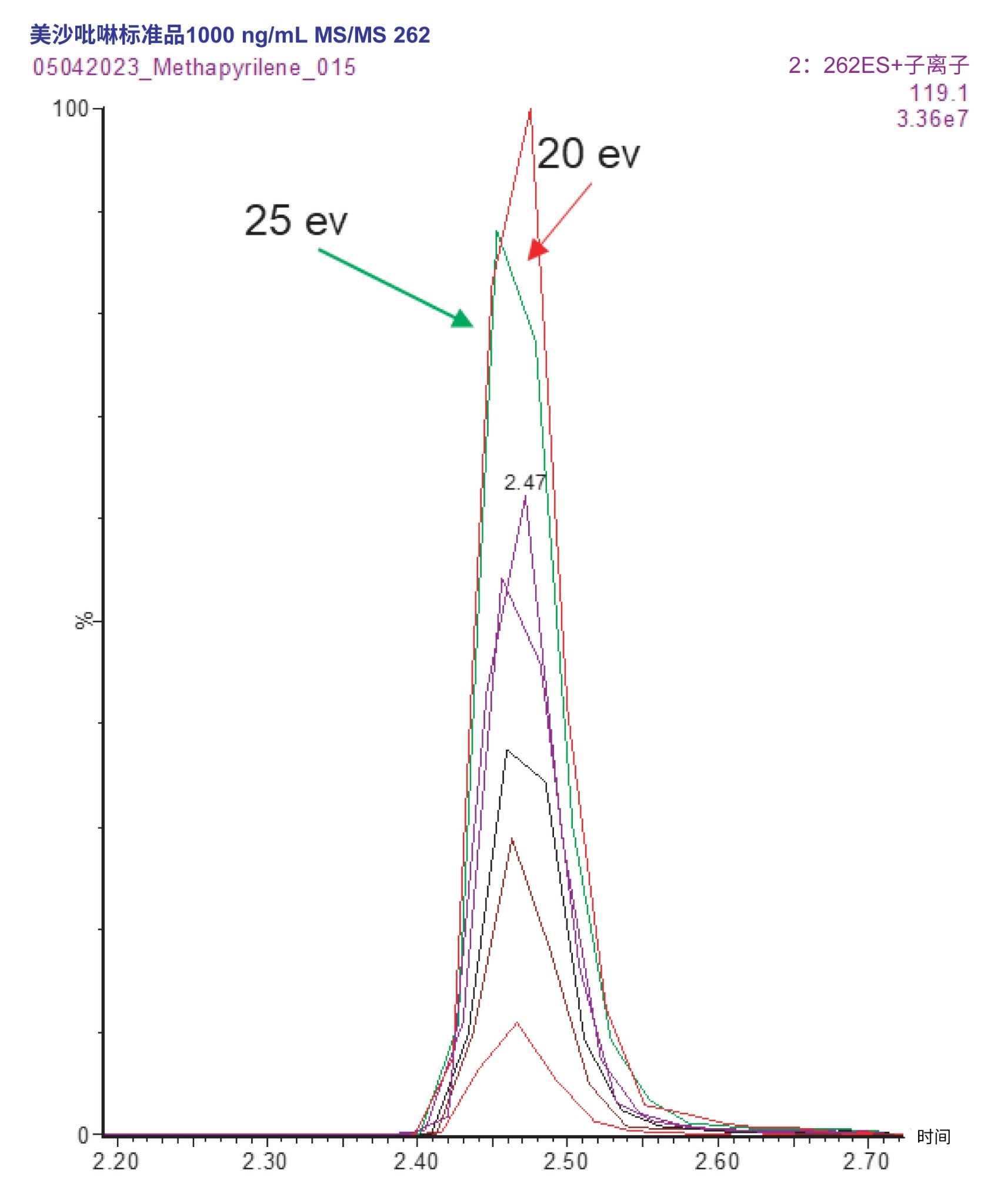
最终通过LC-MS/MS定量血浆中的美沙吡啉,将2 μL萃取样品进样至2.1 × 50 mm CORTECS C18 2.7 µm色谱柱,用5%~40%的甲酸水溶液(0.1%),乙腈(含0.1%甲酸)洗脱时间2.5分钟。色谱柱洗脱液采用正离子ESi在MRM模式下进行监测,通道262.2→119.2,锥孔电压为30 V,碰撞能量为20 eV。
生物分析方法
分析浓度范围的选择取决于DMPK研究的需求,分析方法应始终符合用户需求,值得注意的是,极高灵敏度的分析并非总是必需的。方法开发过程中应考虑分析的动态范围,并与预期的样品浓度范围相匹配。对于一种在典型药物发现的啮齿动物研究中吸收良好并分布广泛的化合物,以10 mg/Kg的剂量给药,预计药物峰浓度为1~7 µg/mL5。 本研究中动物的每日口服剂量(PO)为50或150 mg/kg,因此预期样品中的浓度范围为5~10 µg/mL,因而无需开发灵敏度非常高的分析方法,选择的分析范围为1~1000 ng/mL,这在仪器的定量能力范围内。血浆和尿液样品通过简单的乙腈蛋白沉淀法制得(乙腈:样品=2:1)。在2.1 × 50 mm CORTECS 2.7 µm色谱柱上分析得到的萃取物,以反相模式运行,用5%~40%甲酸水溶液(0.1%)-95%乙腈:水溶液(含0.1%甲酸)的线性梯度进行洗脱,洗脱时间为2.5分钟,流速为600 μL/min。观察到美沙吡啉的保留时间为在tR = 1.69分钟处洗脱。图5展示了使用1/x加权得到的大鼠血浆中美沙吡啉定量的标准曲线,范围为1~1000 ng/mL。外标分析测得的相关系数为0.9986,截距为8.59。图5中的色谱插图显示了1 ng/mL血浆样品和对照空白血浆样品的峰响应。从这些样品中可以看出,空白样品和1 ng/mL样品之间没有观察到明显干扰。
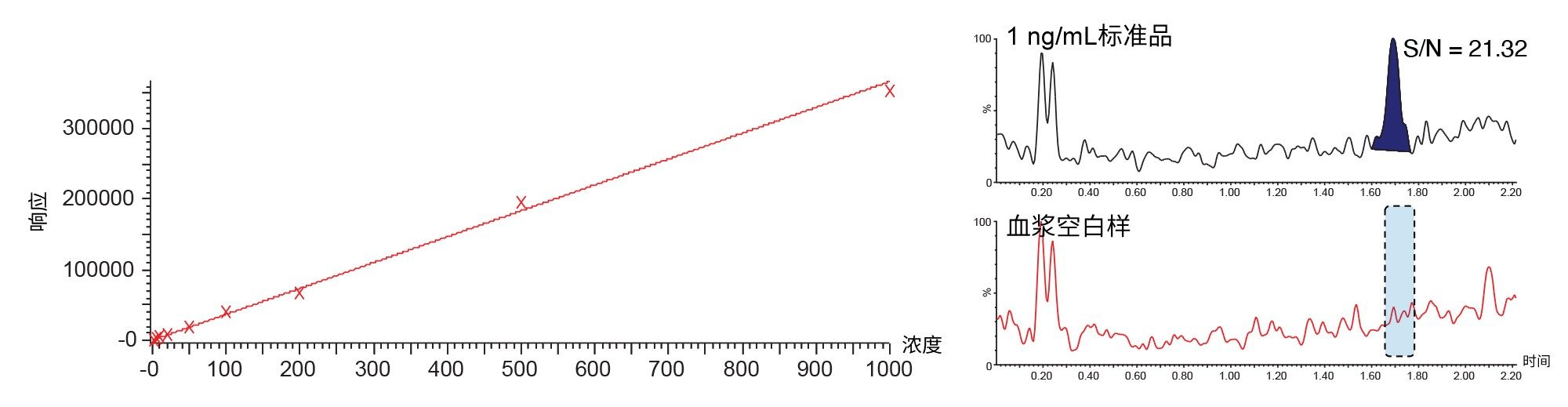
残留评估
为了实现准确、可靠的样品定量,确保分析批次中不会出现交叉污染或前一样品的分析物残留是非常重要的。为了评估这一点,我们在进样分析1000 ng/mL标准曲线标准品后,直接进样分析了一份空白血浆样品。图6展示了添加1000 ng/mL标准品之后获得的血浆空白样峰面积。数据显示,空白血浆样品的S/N值为3.51,而1 ng/mL标准品(图5)产生了一个峰,tR = 1.69 分钟,信噪比(S/N)值为21.3。因此确认分析中没有明显的美沙吡啉残留。
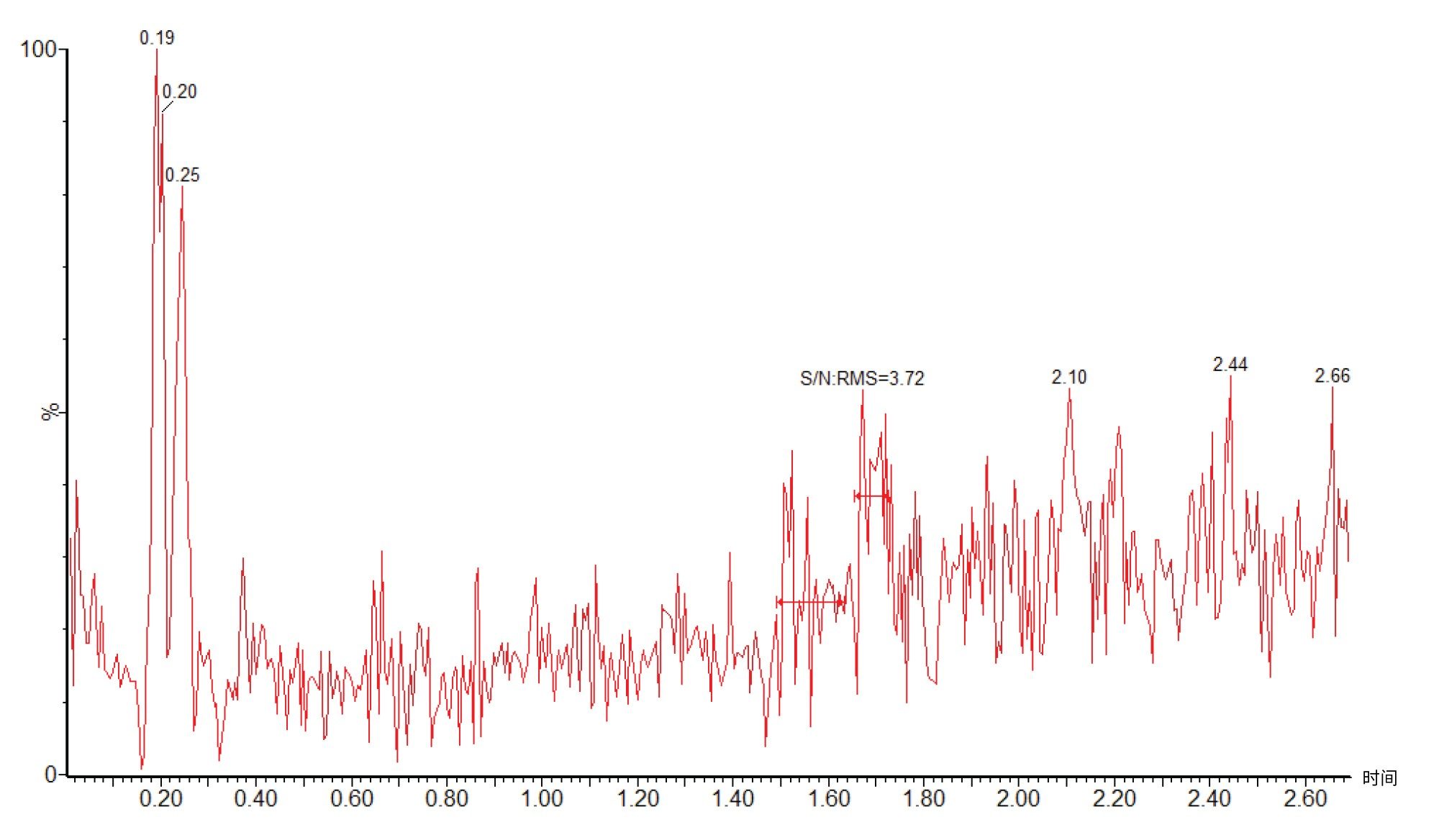
分析验证
美沙吡啉大鼠血浆的检测根据FDA Bioanalytical Method Validation Guidance for Industry(《生物分析方法验证行业指南》,2018)中的说明,经过了为期三天的验证研究,以确定检测限、精密度、准确度、稳定性和可重现性6。在每个分析批次中先绘制一条标准曲线,然后各QC样品重复进样六次,然后再生成第二条标准曲线(单独萃取)。在绘制最终标准曲线之前,通过QC样品中均匀分布的空白血浆萃取物分析,将批次大小增加至96个样品。日间精密度显示,变异系数范围为3.8%~13.3%(分别为1000 ng/mL和1 ng/mL标准品),QC精密度范围为7.2%~10.8%(表3)。通过大鼠尿液进行的分析验证也获得了类似的结果。所有数据均符合FDA生物分析方法验证标准的可接受标准
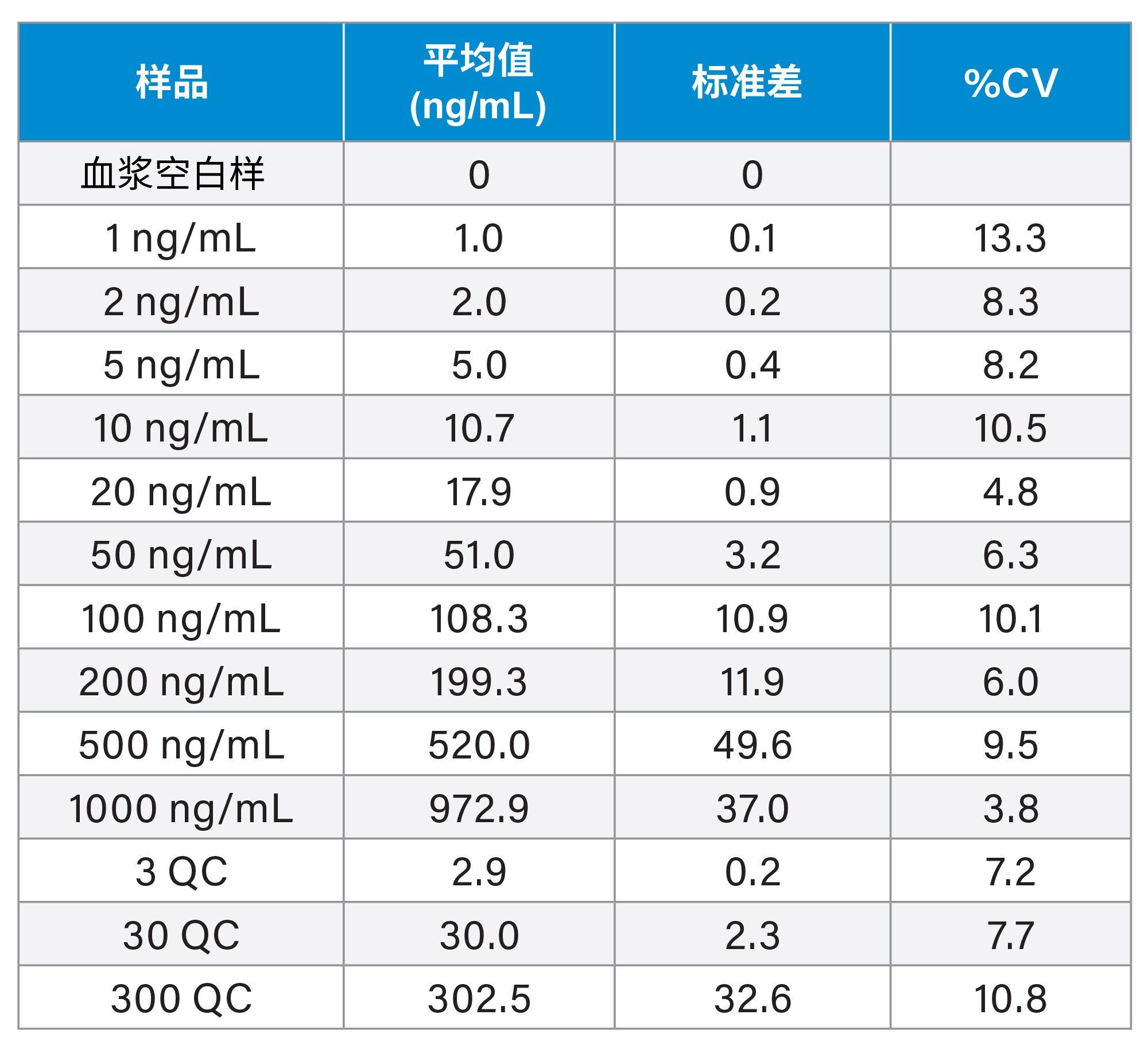
监测基质背景
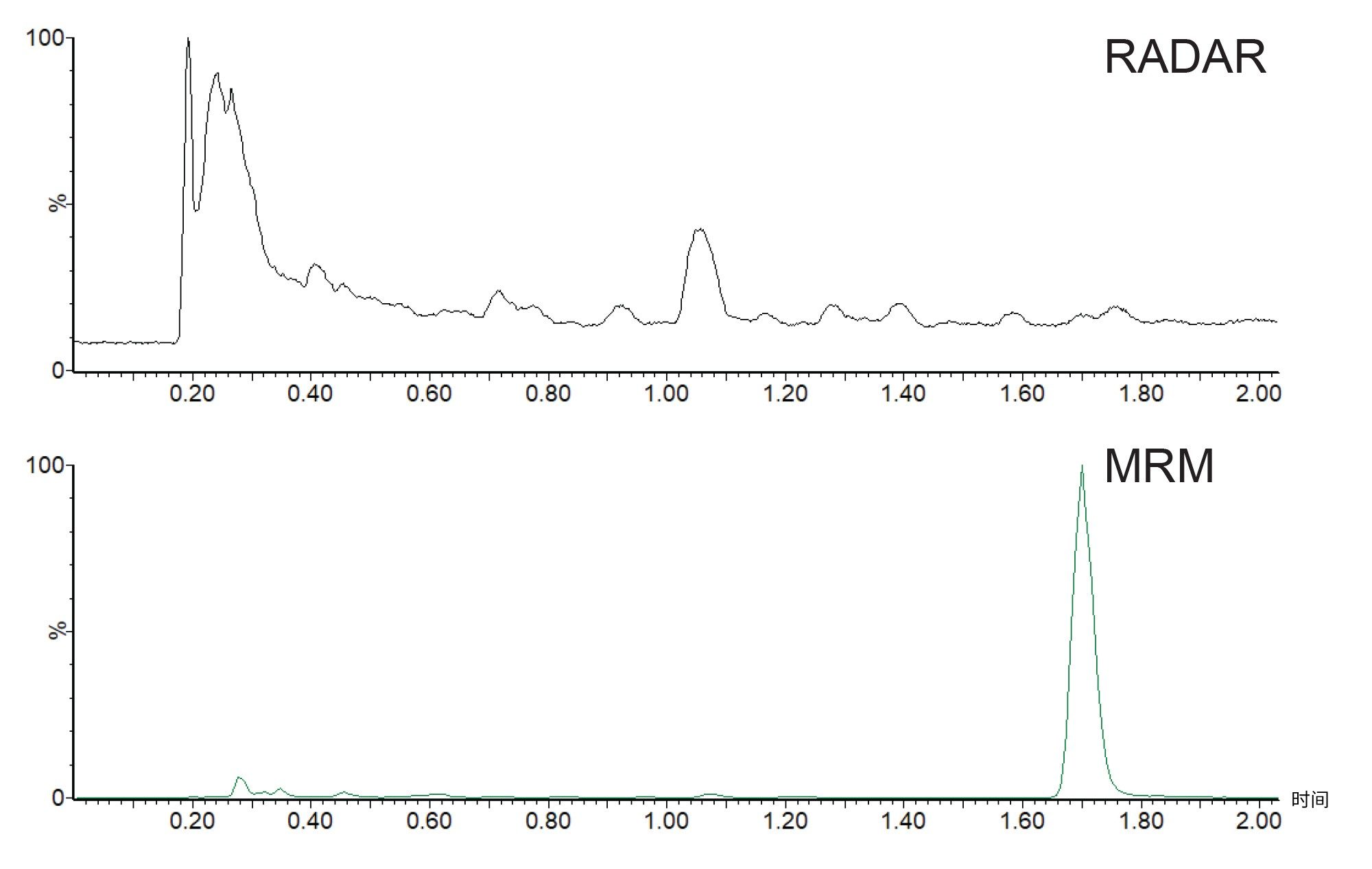
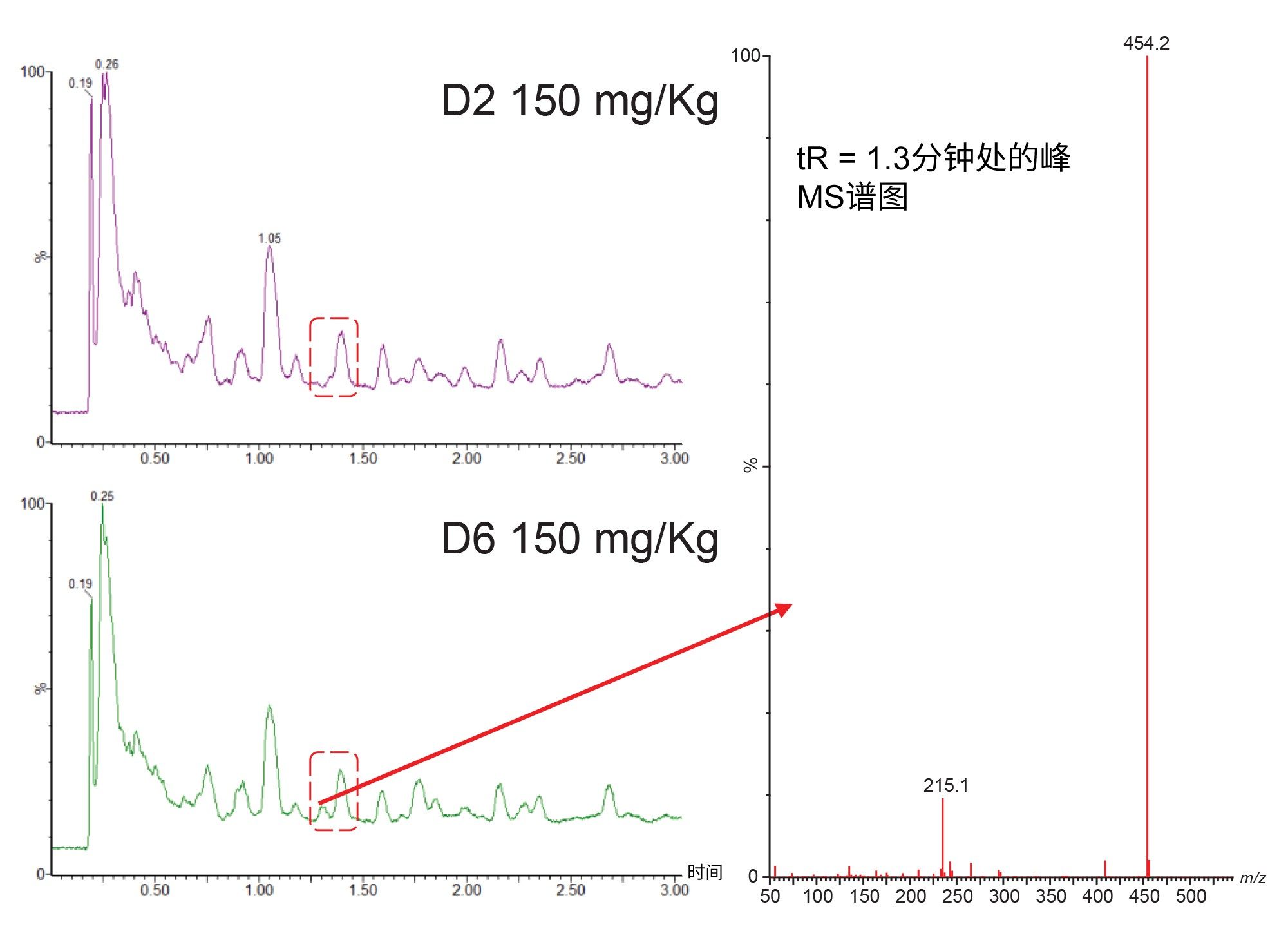
在动物研究中,基质背景信号可能因物种、性别、品系、饮食和年龄而存在显著差异,并且还可能受到给药载体变化的影响。在随机人体临床试验(I-III期)中发现,基质背景信号可能受以下因素的影响:年龄(儿童、老年人)、性别、健康状况、同时接受的治疗,以及饮食和种族。了解基质背景信号的变化如何影响LC-MS/MS方法的稳定性、可靠性和准确度对于更广泛地部署方法至关重要。Waters Xevo系列串联质谱仪搭载RADAR技术,该技术利用创新的T-Wave™碰撞室设计,可在MRM (MS/MS)模式与MS全扫描采集模式之间快速切换。该技术支持同时采集MRM和全扫描数据,而不会对色谱峰的采集点数产生不利影响,并保持分析灵敏度(图7)。图8展示了在第2天和第6天分析尿液样品获得的正离子全扫描LC-MS RADAR数据。从这些数据可以看出,D6样品在tR=1.3分钟处多了一个峰(突出显示为红色框),而D2样品中则没有这个峰。该特征物的RADAR衍生MS谱图在m/z=454.2处产生了一个基峰,在m/z=235.2处出现一个较小的峰(可能是碎片离子),这与美沙吡啉的O-葡糖苷酸代谢物谱图一致。由于该峰的保留时间与美沙吡啉的保留时间明显不同,因此判断这个新峰对尿液中美沙吡啉分析结果的准确度没有影响。正如本例所示,RADAR提供了一些有关口服给药后可能在体内形成的主要代谢物初步迹象,除此之外,RADAR方法还可用于在方法开发过程中监测背景信号以及在常规批次分析过程中监测样品。
结论
LC-MS/MS为定量分析生物体液中的药物及其代谢物提供了高灵敏度方法。本研究开发并验证了一种简单、稳定的MRM分析方法,用于定量分析大鼠血浆和尿液中的美沙吡啉。利用IntelliStart软件可快速优化的母离子、子离子、锥孔电压和碰撞能量,可用于啮齿动物血浆和尿液中美沙吡啉的分析。使用三天方案,在1~1000 ng/mL的标准曲线范围内验证血浆和尿液的分析结果。该方法具有可接受的精密度和重现性。
RADAR可同时采集全扫描数据和MRM数据,监测背景信号,从而实现高效的方法开发、故障诊断排除和临床试验样品分析,同时不会影响定量MRM数据的质量。RADAR技术还有助于其他组分的检测,例如潜在的主要代谢物,有助于为未来的临床前和临床研究提供信息。
参考资料
- Thakur A, Tan Z, Kameyama T, El-Khateeb E, Nagpal S, Malone S, Jamwal R, Nwabufo CK.Bioanalytical Strategies in Drug Discovery and Development.Drug Metab Rev.2021;53(3):434–458.doi: 10.1080/03602532.2021.1959606.Epub 2021 Aug 23.PMID: 34310243.
- Duggan JX.Quantification Below the LLOQ in Regulated LC-MS/MS Assays: A Review of Bioanalytical Considerations and Cautions.Bioanalysis.2019 Apr;11(8):797-814.doi: 10.4155/bio-2018-0261.
- Robert S. Plumb.DMPK研究中的串联四极杆采集模式, 沃特世应用纪要.720008016ZH,2023年9月.
- Graichen ME, Neptun DA, Dent JG, Popp JA, and Leonard TB (1985) Effects of Methapyrilene on Rat Hepatic Xenobiotic Metabolizing Enzymes and Liver Morphology.Fundam Appl Toxicol 5:165–174.
- Molloy B, Mullin L, King A, Gethings LA, Plumb RS, Wilson ID.The Pharmacometabodynamics of Gefitinib after Intravenous Administration to Mice: A Preliminary UPLC-IM-MS Study.Metabolites.2021 11;11(6):379.doi: 10.3390/metabo11060379.
- Bioanalytical Method Validation Guidance for Industry, 2018.https://www.fda.gov/regulatory-information/search-fda-guidance-documents/bioanalytical-method-validation-guidance-industry.
720008082ZH,2023年11月