使用XSelect CSH苯己基柱通过UHPLC-UV-MS分离和检测沙坦类原料药中的叠氮杂质
摘要
近来有关“沙坦类”药物血管紧张素II受体阻滞剂(ARB)的基因毒性杂质问题已促使多家监管机构发出召回通知。这些杂质的安全阈值水平较低,因此迫切需要适当的分析方法。然而,现行美国药典(USP)专论中可能没有能够充分分离活性药物成分(API)杂质的方法。本研究比较了一种新方法与USP专论方法,并展示了替代色谱柱填料XSelect CSH苯己基在分离沙坦类药物混合物(厄贝沙坦、氯沙坦、缬沙坦)和叠氮杂质(5-(4'-(叠氮甲基)-[1,1'-联苯]-2-基)-1H-四唑)方面的潜力。将ACQUITY Arc系统与PDA和ACQUITY QDa质谱检测器联用,所有化合物均获得了更高的选择性和分离度,由此开发出一种快速的3 min等度方法,使每种化合物都表现出良好的MS线性。
优势
- 使用XSelect CSH苯己基柱提高沙坦类药物和叠氮杂质的分离度
- 使用LC-UV-MS准确分析沙坦类原料药中的叠氮杂质
- 使用3 min等度方法快速、可重现地定量16 ng/mL–50 µg/mL的叠氮杂质
简介
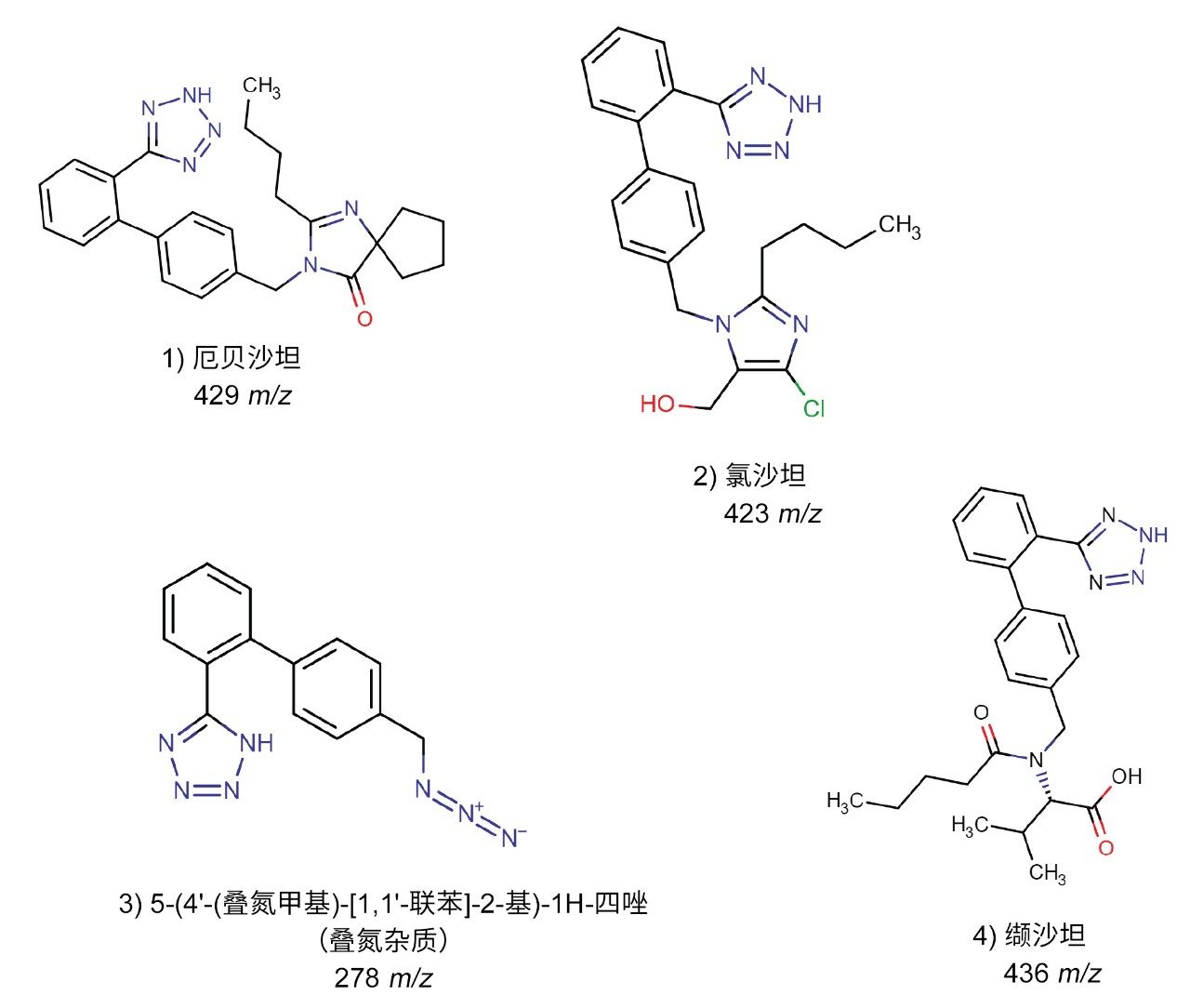
厄贝沙坦、氯沙坦和缬沙坦为血管紧张素II受体阻滞剂(ARB),用于治疗高血压和糖尿病肾病(肾病)1。因怀疑这些“沙坦类”药物中存在基因毒性叠氮杂质5-(4'-(叠氮甲基)-[1,1'-联苯]-2-基)-1H-四唑,监管机构于2021年6月发布了召回通知2。 这种叠氮杂质是各活性药物成分(API)合成途径的中间体,由相似的骨架结构组成。如图1所示,上述四种化合物均含有与苯基键合的四唑环,并在邻位结合另一个苯基。不同化合物的区别体现在第二个苯环的对位结构上,需要采用合适的分析方法准确检测和定量叠氮杂质和沙坦类API。如果化学结构相似,这一工作将更具挑战性。
在本研究中,我们介绍了采用UV-MS双重检测的UHPLC方法,该方法使用XSelect CSH苯己基柱,在3 min内快速准确地分析叠氮杂质5-(4'-(叠氮甲基)-[1,1'-联苯]-2-基)-1H-四唑以及沙坦类API(厄贝沙坦、氯沙坦和缬沙坦)。将配备PDA检测器的ACQUITY Arc系统与ACQUITY QDa质谱检测器联用。这种快速、简单的方法采用等度条件以及可兼容MS的流动相,可完全分离四种化合物。UV检测与MS检测相结合有利于对叠氮杂质和API进行准确测定和质量数确认,并具有更高的分析灵敏度,使用1 µL的进样体积时,叠氮杂质的检测下限低至16 ng/mL。
实验
样品描述
使用50:50乙腈:水作为样品稀释剂,制得浓度为1 mg/mL的四种分析物储备液。随后的所有稀释均使用50:50乙腈:水作为稀释剂。整个检测过程中的样品浓度各不相同。
液相色谱条件
|
液相色谱系统: |
配备2998 PDA检测器和ACQUITY QDa质谱检测器的ACQUITY Arc |
|
检测条件: |
UV 230 nm |
|
分析物的SIR(图1) |
|
|
样品瓶: |
LCMS认证透明玻璃样品瓶,容积2 mL(部件号:600000751CV) |
|
色谱柱: |
XSelect BEH C18色谱柱, 3.0 × 50 mm, 2.5 µm(部件号:186006033) |
|
XSelect CSH苯己基柱, 3.0 × 50 mm, 2.5 µm(部件号:186006129) |
|
|
柱温: |
30 °C |
|
样品温度: |
10 °C |
|
进样体积: |
1 µL |
|
流速: |
1.7 mL/min – 由USP专论方法缩放而来 |
|
0.85 mL/min – 方法开发流速 |
|
|
流动相A: |
水 |
|
流动相B: |
乙腈 |
|
流动相C: |
50:50:0.1(乙腈:水:乙酸) USP专论流动相 |
|
流动相D: |
2%甲酸的水溶液 |
质谱条件
|
质谱系统: |
ACQUITY QDa |
|
电离模式: |
ESI+下的SIR |
|
采集范围: |
见图1 |
|
毛细管电压: |
1.5 kV |
|
锥孔电压: |
15 V |
数据管理
|
色谱软件: |
Empower 3 Feature Release 4 |
结果与讨论
图1中化合物的初步方法开发工作主要是创建一种通用方法,能够分离、检测和定量沙坦类药物和叠氮杂质。基于这些原因,我们使用配备PDA检测器的ACQUITY Arc系统进行分析,并与ACQUITY QDa质谱检测器集成以进行质量数确认。缬沙坦的USP专论方法作为方法开发起点进行了考察,因为厄贝沙坦和氯沙坦专论方法都在流动相中使用了与MS检测不兼容的磷酸和磷酸盐缓冲液。缬沙坦的USP专论方法采用乙腈:水:乙酸的组合作为流动相,是唯一能够兼容MS检测的沙坦类药物专论方法。
分析时,按照USP专论中所述的方法制备四种化合物的储备液3。 使用XBridge BEH C18色谱柱(3.0 × 50 mm,2.5 µm;此规格由USP专论方法缩放而来),对0.2 mg/mL API和0.02 mg/mL叠氮杂质执行单标进样,并进样四种化合物指定浓度的混合物。LC和MS的全部详细信息见实验部分。图2显示了使用该方法获得的UV色谱结果。
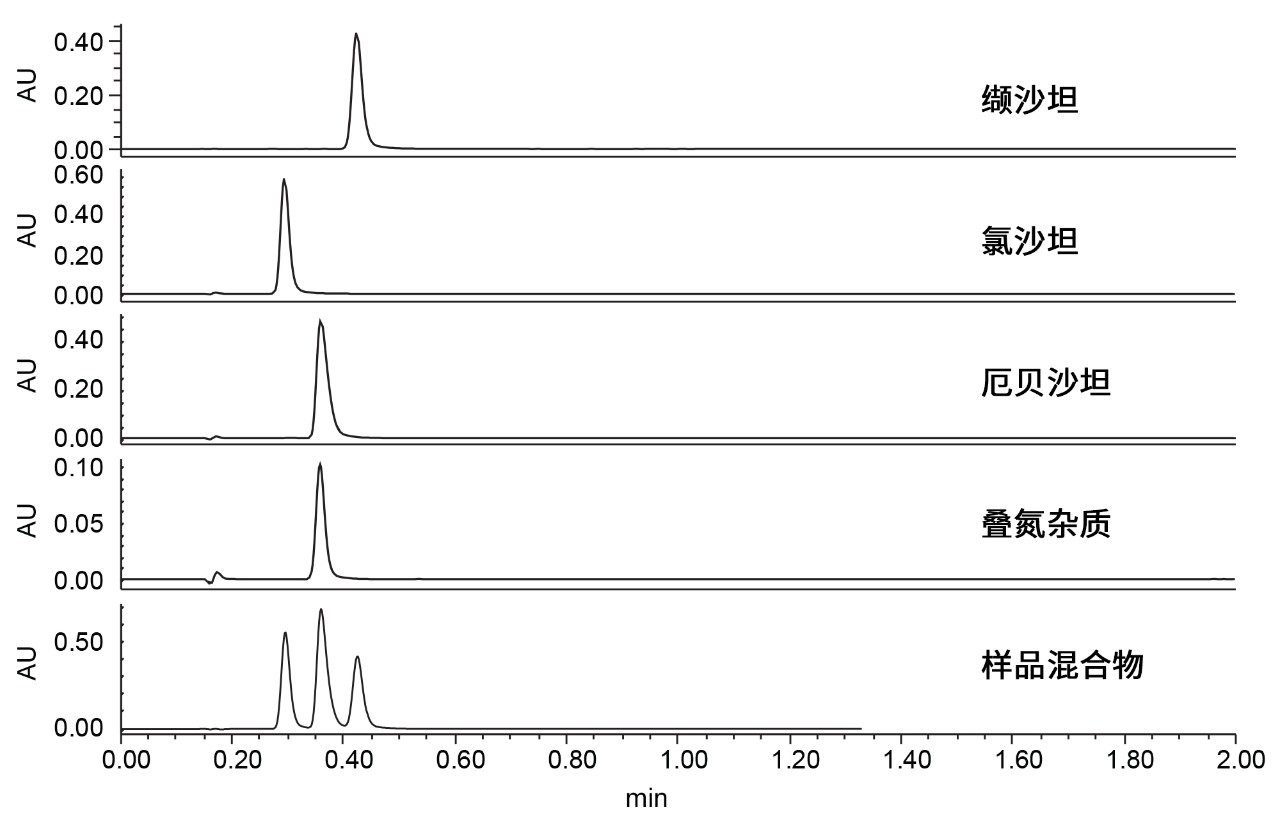
从图2可以看出,使用缩放的USP专论方法和XSelect XBridge BEH C18色谱柱时,三种沙坦类药物和叠氮杂质的分离不充分,叠氮杂质与厄贝沙坦峰共流出。此结果说明,尚未开发出能够完全分离杂质和沙坦类药物的通用方法,还需要进一步的方法开发。考虑到这四种化合物具有密切相关的多环结构,我们接下来选择XSelect CSH苯己基柱进行测试。这款色谱柱与XBridge BEH C18色谱柱相比采用了不同的基质颗粒和键合相。CSH颗粒与BEH颗粒相似,二者均为杂化颗粒;但前者颗粒上保留少量正电荷,而BEH颗粒上没有。此少量电荷有两种作用。首先,由于弱离子排斥效应,少量正电荷可改善碱性分析物在低pH条件下的峰形。其次,颗粒上的正电荷在适当情况下可以充当弱阴离子交换剂,从而对酸性探针具有不同的选择性。苯己基键合相与C18键合相的不同之处在于,键合相与分析物之间可能发生次级π-π相互作用,这种相互作用被证明在分析含有多个苯环的化合物(例如沙坦类药物)时是有利的。
使用这款XSelect CSH苯己基柱,我们可以在沙坦类药物和叠氮杂质的分离中获得更出色的选择性和更高的分离度。还能进一步优化方法,将等度方法运行时间大幅缩短至3 min,如图3所示。另外还发现使用甲酸作为流动相改性剂足以实现所需的分离效果。
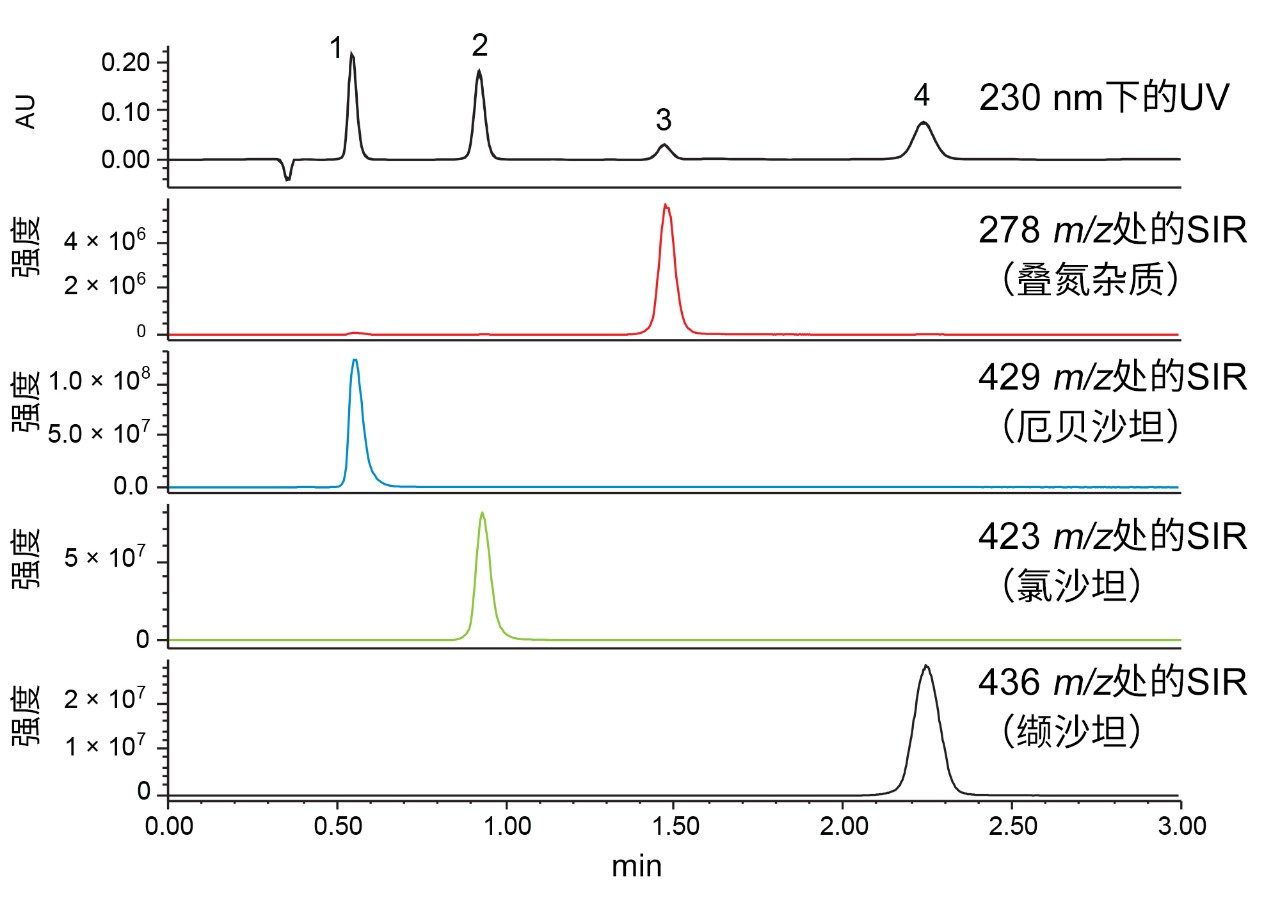
图3.使用XSelect CSH苯己基柱(3.0 × 50 mm, 2.5 µm)分析叠氮杂质、厄贝沙坦、氯沙坦和缬沙坦获得的UV和SIR色谱图。利用配备PDA检测器的ACQUITY Arc系统进行等度分离,并与ACQUITY QDa联用进行质谱检测,所用流速为0.85 mL/min,柱温为30 °C,且采用添加甲酸作为改性剂的流动相(40:60乙腈:水)。
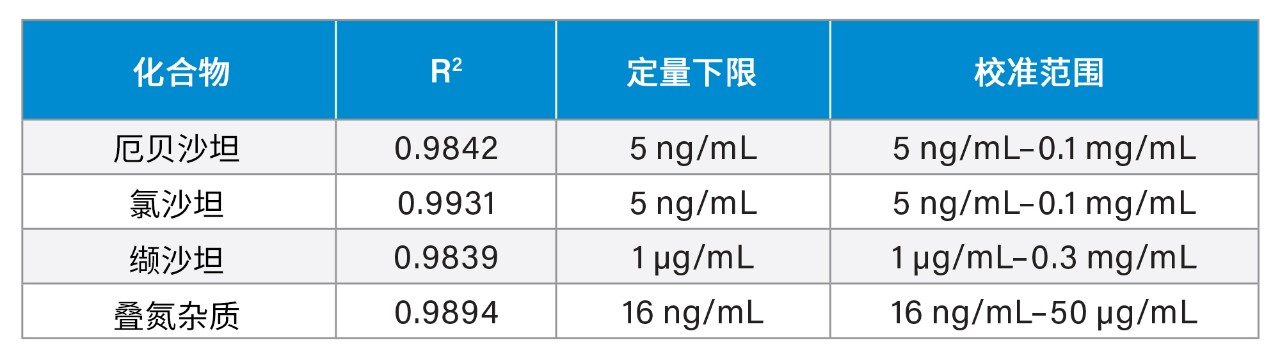
优化液相色谱方法后,使用ACQUITY QDa质谱检测器评估沙坦类药物和叠氮杂质的MS灵敏度和线性。为所有四种化合物生成校准曲线(n = 3)。表1突出显示了MS定量性能,包括定量下限、线性回归(R2)、校准曲线范围。为确认叠氮杂质的MS准确度,用50 ng/mL样品评估了回收率/准确度和重现性。测得的平均%回收率(n = 9)为97.4%,%RSD为4.2%,完全符合建议的回收率(85~115%)和RSD标准。
结论
本研究成功开发出一种快速、通用的LC-UV-MS方法,可准确且可重现地分析叠氮杂质(5-(4'-(叠氮甲基)-[1,1'-联苯]-2-基)-1H-四唑)和沙坦类API。与过去使用的C18色谱柱相比,XSelect CSH苯己基柱具有优异的选择性,可有效分离氯沙坦、缬沙坦、厄贝沙坦和叠氮杂质。将配备PDA检测器的ACQUITY Arc系统与ACQUITY QDa质谱检测器联用,可实现快速、准确的峰确证。总而言之,这种概念验证方法为测定沙坦类API中的叠氮杂质5-(4'-(叠氮甲基)-[1,1'-联苯]-2-基)-1H-四唑提供了一种简单的解决方案,运行时间不超过3 min。
参考资料
- Angiotensin II Receptor Blockers.Mayo Clinic Website.Accessed 30-Aug-2021.https://www.mayoclinic.org/diseases-conditions/high-blood-pressure/in-depth/angiotensin-ii-receptor-blockers/art-20045009.
- Government of Canada Recalls and Safety Alerts.Multiple Lots of Irbesartan, Losartan, and Valsartan Drugs Recalled Due to Azido Impurity.Accessed 16-Aug-2021.https://healthycanadians.gc.ca/recall-alert-rappel-avis/hc-sc/2021/75715a-eng.php.
- USP Monograph Conditions Valsartan Tablets.USP43-NF38-4579, USP42-NF37-4539, USP41-NF36 2S-8984.Accessed via USP-NF mobile app 19-July-2021.
720007369ZH,2021年9月