
本应用纪要介绍了使用SmartMS赋能的新款紧凑型台式LC-MS系统鉴定尼古丁及其相关杂质的高效且简便易用的工作流程。使用waters_connect软件平台内的UNIFI应用程序鉴定并报告API(活性药物成分)及相关杂质。利用ACQUITY RDa检测器在碎裂模式下的全扫描功能生成的碎片离子信息进一步确认分配结果。通过提高碎裂锥孔电压获取更多结构信息。
杂质分析是药物开发过程的关键部分。未知杂质的鉴定是优化药物疗效和安全性的关键因素。为鉴定API中存在的杂质提供成功的解决方案是一项复杂并且具有挑战性的任务。高分辨率质谱(HRMS)是一种常用的分析技术,可以准确鉴定API中存在的杂质;但该技术需要分析人员具备丰富经验和高水平专业知识才能解决相关的分析难题。ACQUITY RDa检测器具有自动设置和校准功能,使拥有不同程度专业知识的科学家都可以实现精确质量数测定。因此,非专家水平的用户也可以使用HRMS,让科学家能够获得更深入的分析信息。

尼古丁是一种天然产生的手性生物碱,在娱乐消遣方面广泛用作兴奋剂和抗焦虑剂。作为药物使用时可以减轻戒断症状,从而达到戒烟目的。电子烟和尼古丁口香糖可以替代吸烟体验,所用的尼古丁提取自烟草,其纯度可能因制造商和等级(例如药品级)而异。美国药典(USP)级别的尼古丁要求单一杂质量少于0.5% (5 mg/g),总杂质量少于1% (10 mg/g)。欧洲药典专论1452中规定的尼古丁杂质有:尼古丁-N-氧化物、可替宁、去甲烟碱、新烟草碱、麦斯明、新烟碱和β-二烯烟碱。
尼古丁和相关生物碱的分析可采用多种方法(GC、NPD和MS)1-4。 尼古丁-N-氧化物等尼古丁相关化合物在GC分析所需的温度下热稳定性差,某些目标化合物(例如去甲烟碱)可能存在严重的进样器残留问题1,2,4。 使用配备UV检测器的HPLC系统可以解决这些问题,但该方法的灵敏度有限,无法区分潜在的共流出化合物。因此需要采用HRMS等分析技术来克服这些问题,该技术通常需要由经验丰富的用户来操作仪器。
对于非HRMS专家级用户的科学家而言,具有SmartMS功能的ACQUITY RDa检测器是实现精确质量数测定和收集深度分析信息的理想选择。此外,waters_connect软件平台在合规性框架内自动采集、处理和报告结果,可确保数据完整性。使用碎裂模式下的全扫描功能同时采集低能量谱图和高能量谱图,获取碎片离子信息,从而提高化合物鉴定的可信度。
将新型ACQUITY RDa检测器与ACQUITY UPLC I-Class PLUS系统联用,根据USP专论方法使用以极性嵌入的封尾十八烷基硅烷键合无定型有机硅胶聚合物为固定相的R(4.6 mm × 150 mm, 5 µm)色谱柱分析尼古丁中的杂质。ACQUITY RDa检测器是一款紧凑的台式飞行时间(Tof)质谱仪,质量分辨率>10,000 FWHM,适用于常规的精确质量数测定。该系统可同时采集全扫描数据和碎裂模式下的全扫描数据(非数据依赖型采集模式)。UNIFI应用程序是一种简便易用且可定制的平台,利用精确质量数、保留时间和碎片离子信息快速搜索可定制的特定应用数据库以鉴定化合物。图1展示了ACQUITY RDa检测器。
用水配制杂质混标的储备液(100 ppm)。配制10 mg/mL二水二酒石酸烟碱样品溶液,并以水作为稀释剂,用杂质混标加标,使最终溶液浓度为100 ppb。
|
液相色谱系统: |
ACQUITY UPLC I-Class PLUS |
|
检测条件: |
TUV,在260 nm下检测 |
|
样品瓶: |
全回收样品瓶 |
|
色谱柱: |
XBridge Shield RP18, 4.6 × 150 mm, 5 µm |
|
柱温: |
30 °C |
|
样品温度: |
20 °C |
|
进样体积: |
20 µL |
|
流速: |
1.000 mL/min |
|
流动相A: |
25 mL 1 M乙酸+6 mL氨水溶液,pH 10 |
|
流动相B: |
乙腈 |
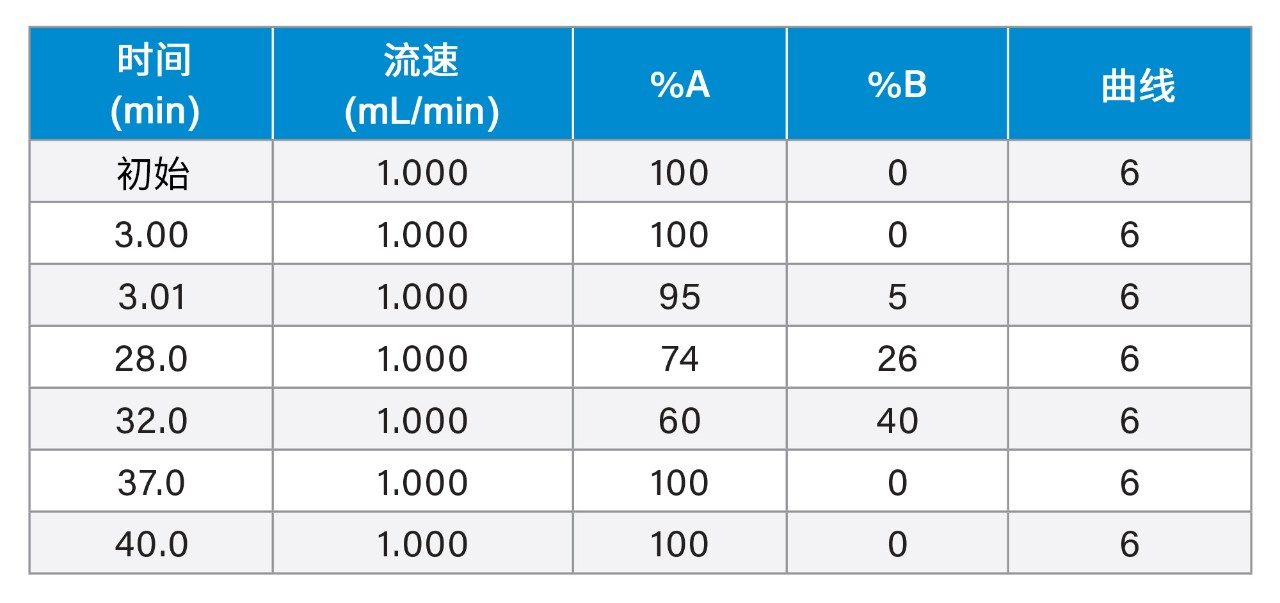
|
质谱系统: |
ACQUITY RDa检测器 |
|
电离模式: |
碎裂模式下的全扫描(伪MSE采集) |
|
采集范围: |
50–2000m/z |
|
毛细管电压: |
1.5 kV |
|
碎裂锥孔电压: |
50-80 V |
|
锥孔电压: |
30 V |
|
极性: |
正离子 |
|
扫描速率: |
5 Hz |
|
脱溶剂气温度: |
550 °C |
|
信息学软件: |
waters_connect v1.9.12 |
ACQUITY RDa检测器利用精确质量数工作流程测量精确质量数,以实施鉴定并制定明智决策。本研究展示了用于杂质分析的UNIFI软件应用工作流程,该工作流程也可以扩展至降解研究,如图3所示。
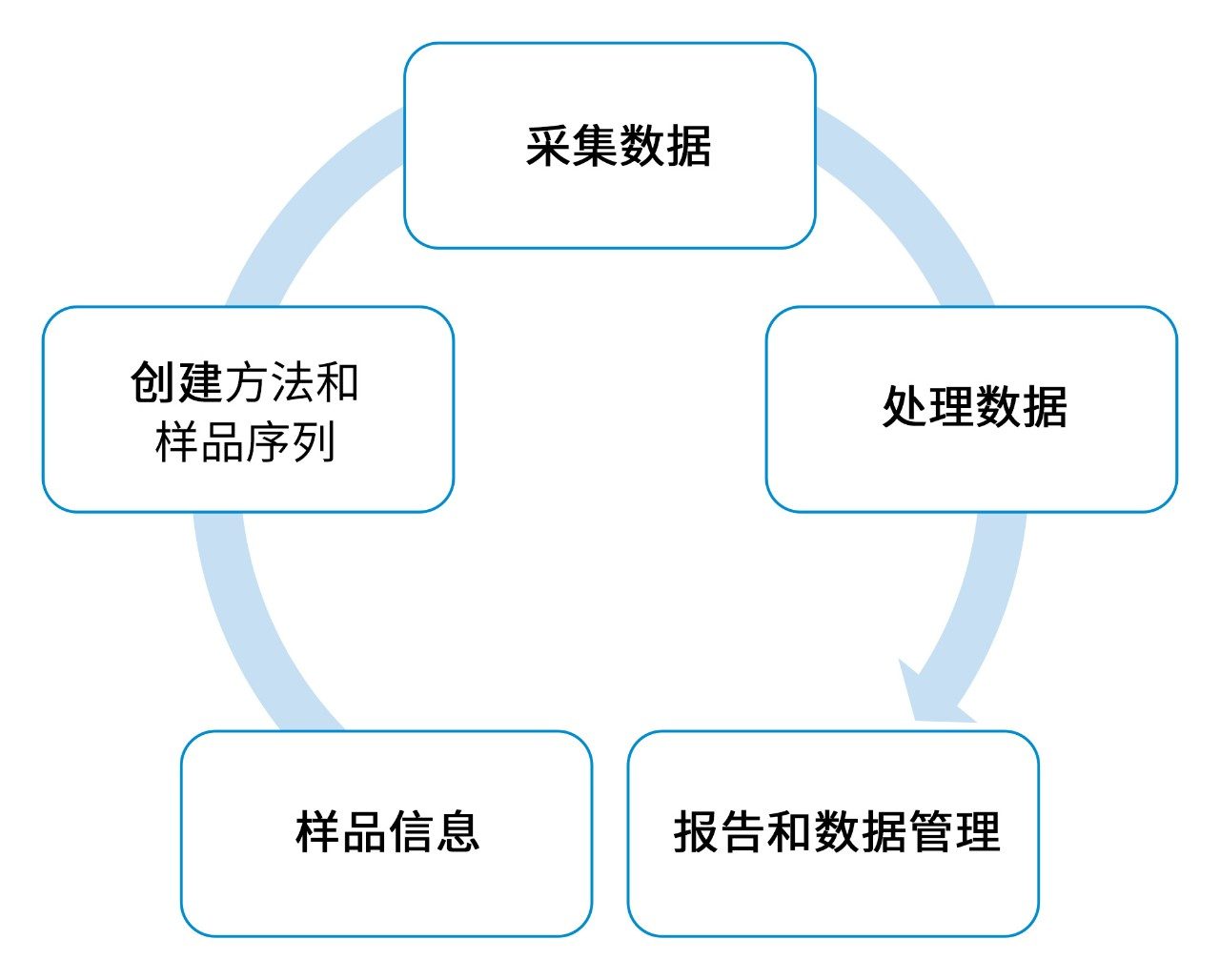
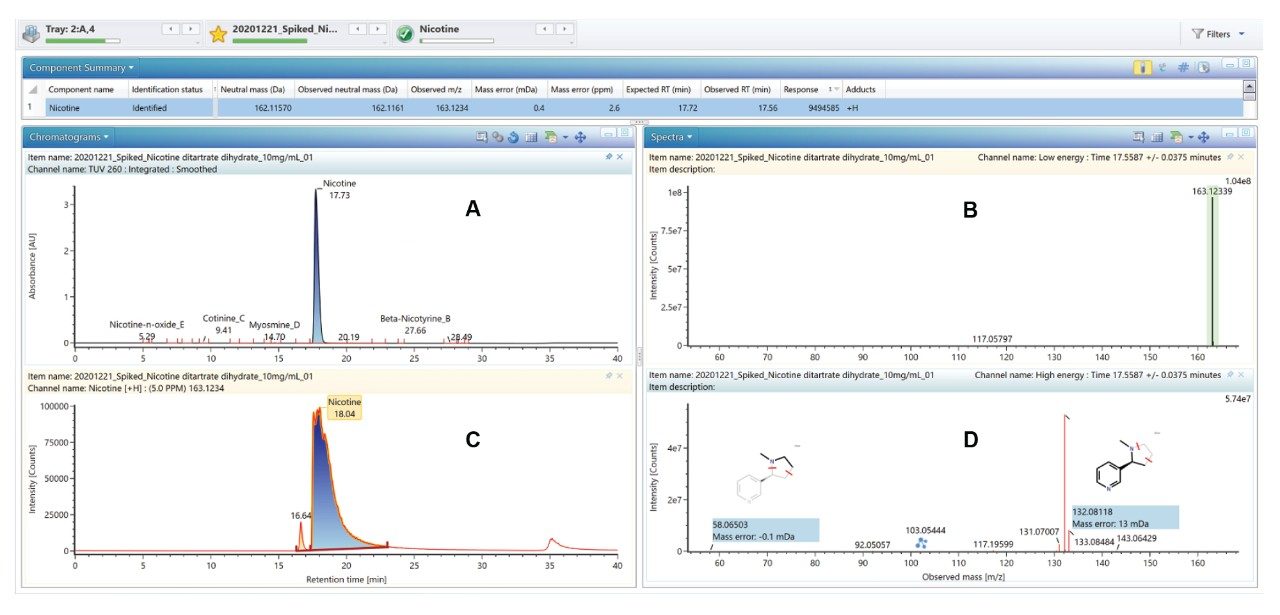
如图4所示,UV采集与MS检测同时进行,因此能够比较两种迹线。
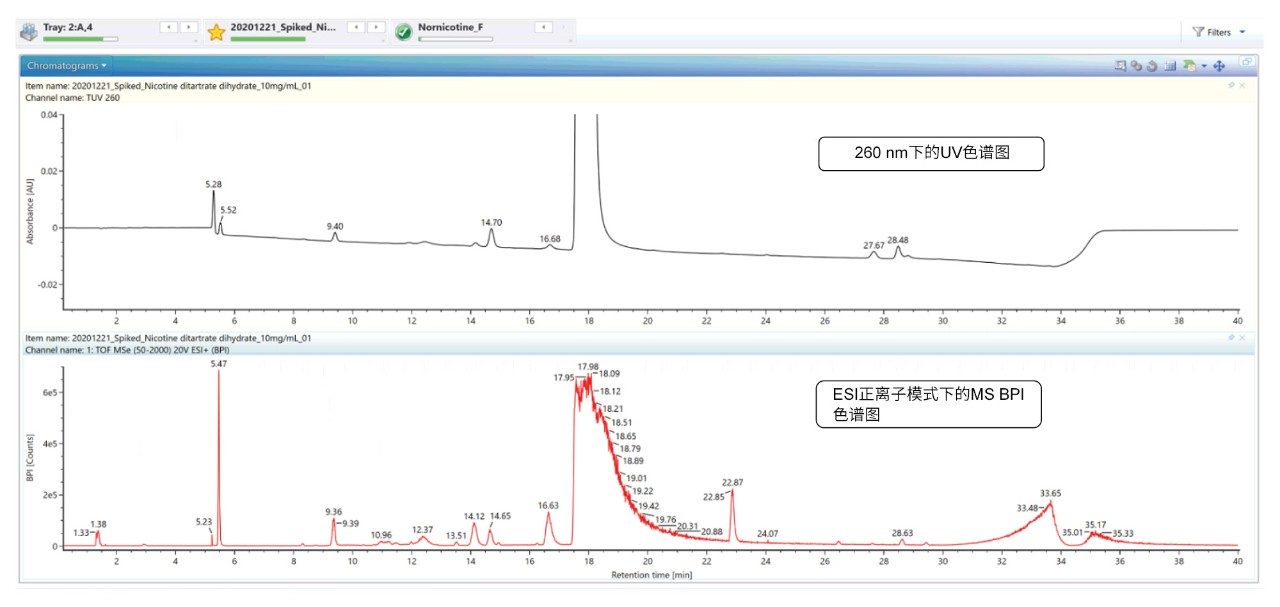
在ACQUITY RDa检测器上利用碎裂模式下的全扫描功能采集添加有杂质混标(100 ppb)的尼古丁API样品(10 mg/mL)数据,其中低能量和高能量通道分别包含母离子和碎片离子信息(图5)。
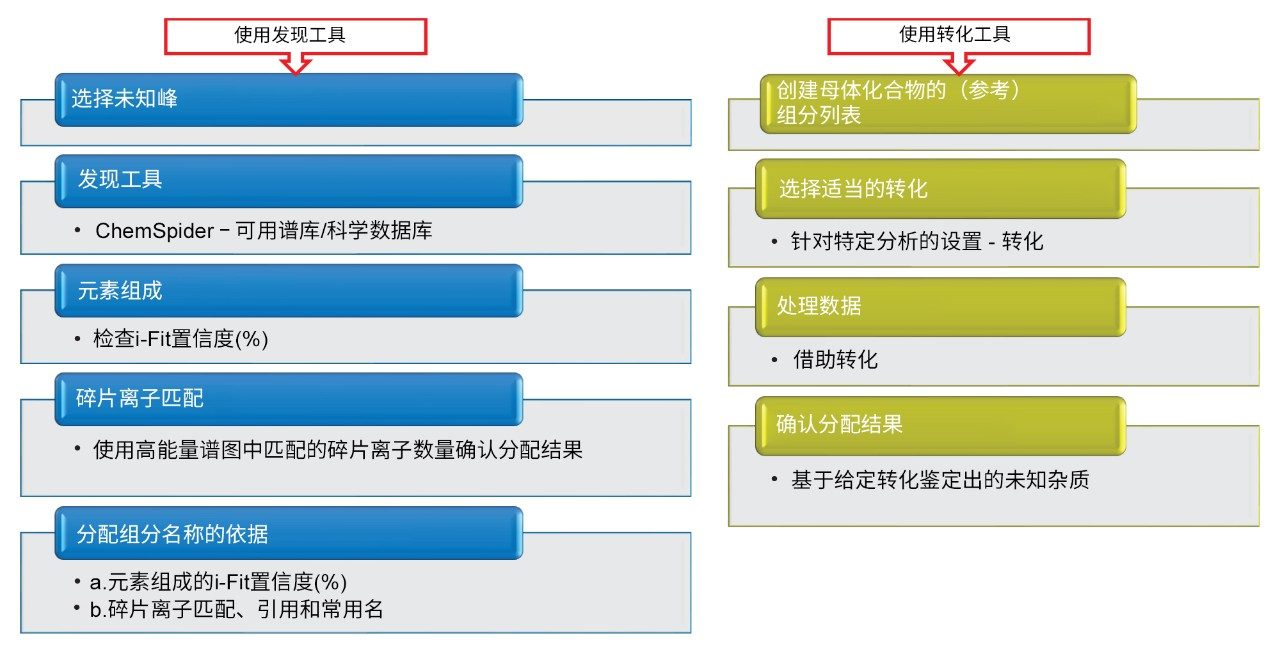
本应用纪要介绍了两种不同的方法;这两种方法分别使用“发现工具”和“转化工具”来鉴定未知杂质,如图6所示。
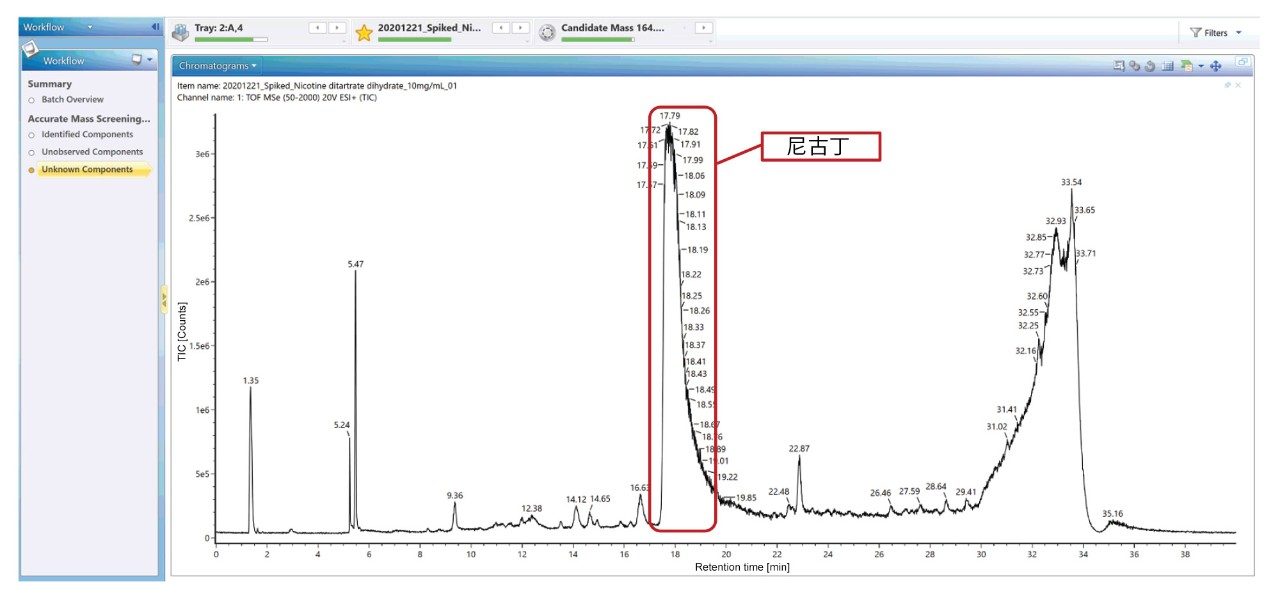
集成的发现工具使用户能够解析未鉴定出的峰,并快速搜索结构数据库ChemSpider,推测性鉴定未知化合物。如图7所示,使用发现工具可以在17.57 min的RT处鉴定出尼古丁峰。
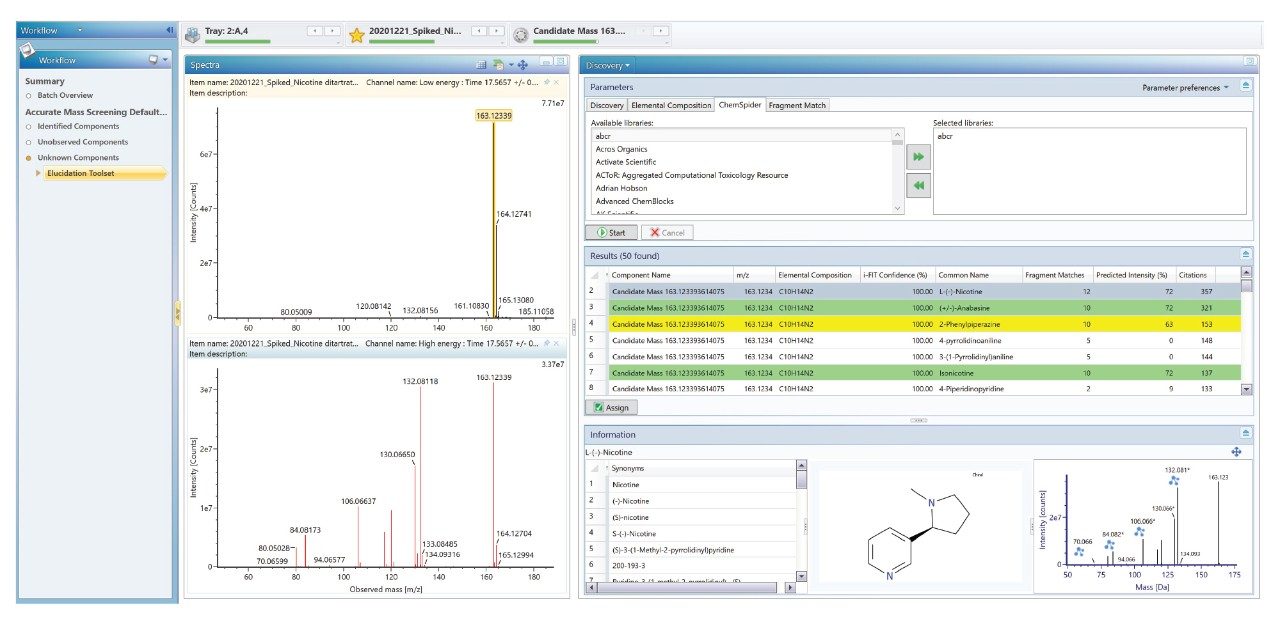
发现工具会获取17.57 min处色谱峰的精确质量数,提出元素化学式,并在选定的ChemSpider库中搜索可能的匹配。本例中发现了十二个数据库匹配结果在所用的偏差范围内。此外,发现工具还会对提出的数据库匹配结果(使用.mol文件)执行计算机模拟碎裂,并将产生的理论碎片离子与获得的碎片离子谱图进行比较。发现的第一种候选物是尼古丁,其建议的碎片离子分配结果与高能量谱图相匹配,如图8所示。
使用发现工具鉴定出未知杂质后,即可将该杂质输入科学数据库中以备常规分析使用。图9展示了通过科学数据库对尼古丁及其相关杂质的鉴定。
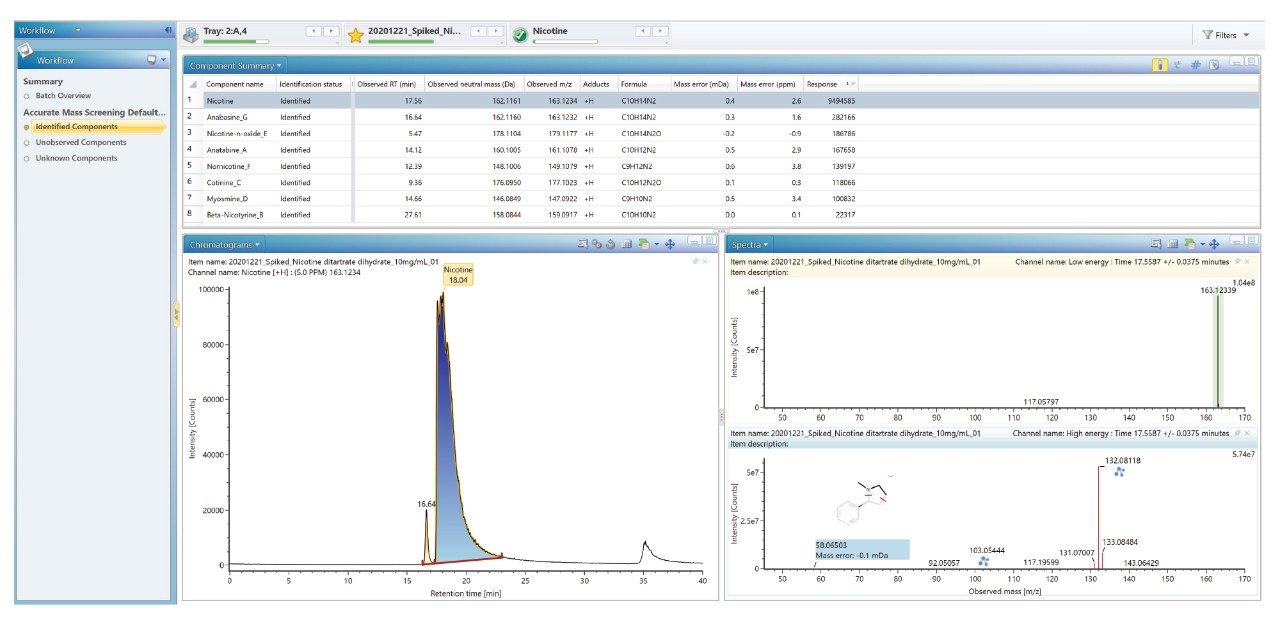
此外,还可以使用发现工具来确定API的可能鉴定结果,使用转化工具来鉴定杂质。本研究使用UNIFI应用程序中内置的转化工具成功鉴定出与API相关的杂质,包括氧化、还原和脱烷基化杂质。疑似杂质显示在组分概要中,其中列出了与预测杂质的m/z相匹配的所有峰(图10)。还显示了色谱图和质谱图,高能量谱图中的自动碎片离子分配结果带有蓝色图标(图10)。如图10左侧所示,该工具结合杂质分析工作流程来鉴定与API相关的未知杂质是一种高效的方法。
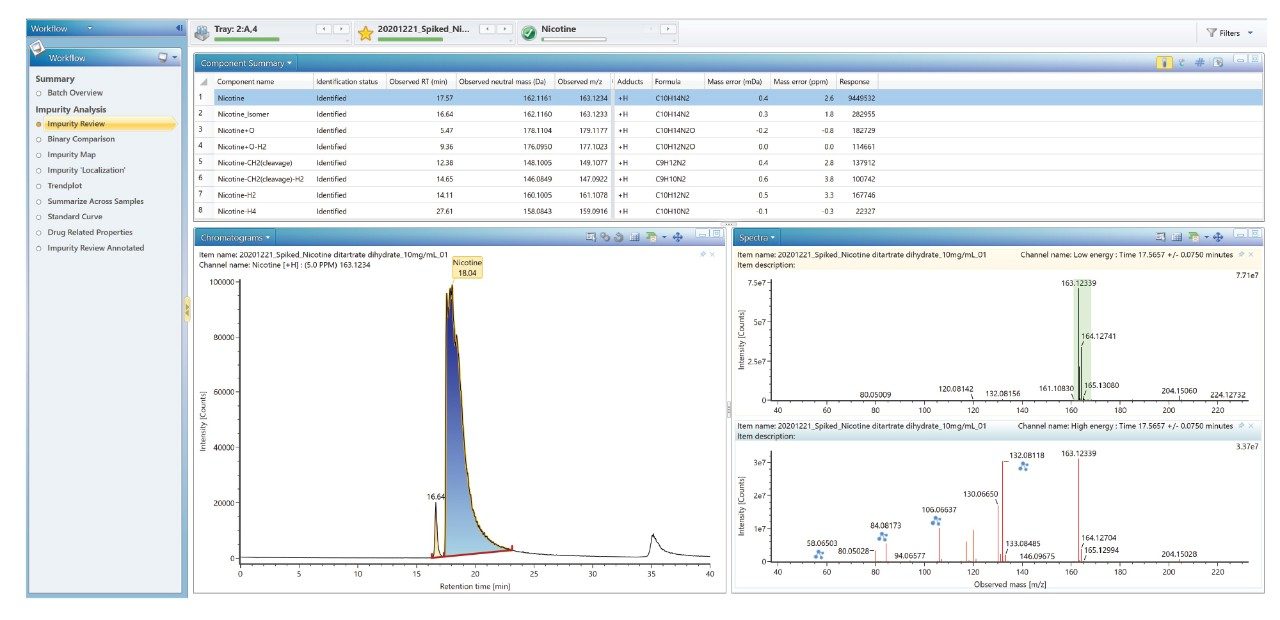
使用ACQUITY RDa检测器与waters_connect软件平台来鉴定二水二酒石酸烟碱的所有相关物质。
使用ACQUITY RDa检测器、配备TUV的ACQUITY UPLC I-Class PLUS系统和waters_connect软件平台成功鉴定出尼古丁及其相关杂质。通过结合精确质量数工作流程,科学家们能够监测API及其相关杂质的水平。这使他们能够评估和控制这些类型的样品组,从而在制药行业内确定质量标准限值。利用搭载UNIFI应用程序的waters_connect软件平台,基于质量数测定和碎片离子分配结果,以高可信度自动鉴定尼古丁及其相关杂质。
Waters ACQUITY RDa检测器结合常规工作流程支持化学家鉴定和表征杂质,使他们能够制定明智且有影响力的决策。
720007232ZH,2021年5月