
本应用纪要介绍了成功验证Waters ACQUITY UPLC I-Class PLUS系统与Xevo TQ-S micro质谱仪联用分析虾组织中四环素、磺胺类药物、甲氧苄氨嘧啶、奥美普林和氨苯砜的结果。
兽药在畜牧业和水产养殖业中用于治疗或预防疾病,有时也用于促进牲畜生长。但是,如果未遵守规定的休药期,牛奶、鸡蛋和肉类等食用产品中可能会存在不安全的抗生素残留或其代谢物。为满足日益增长的需求,虾和其他海产品通常在水产养殖场进行养殖,许多动物被饲养在相对狭小的空间内,因此更容易患病。为保护动物健康以及确保生产并增加产量,抗生素被大量使用。这些抗生素在动物源性食品中的残留是一项主要问题,因为它们对消费者的健康有害,并可能导致病原体产生耐药性1。
监管机构通过规定最大残留量(MRL)或禁止使用多种物质来监管兽药的使用,从而确保食品安全并促进各国之间的贸易。欧盟规定了许多物质的MRL,适用于所有食品生产物质;磺胺类药物的MRL用磺胺类药物组内所有物质的总残留量表示,四环素的MRL则与母体药物及其4-差向异构体(强力霉素(DC)除外)的总和有关2。 氨苯砜、地美环素和奥美普林在欧盟未获准用于食品动物,因此未规定相应的MRL,尽管氨苯砜的建议浓度(RC)为5 μg/kg3。 当禁止使用某种物质时,CCα和CCβ限值应始终处于合理范围内的最低水平(ALARA)。
严格的监管与有效的执法、调查和检查活动相结合,可确保世界各地安全有效地使用兽药。例如,欧盟国家必须实施残留物监测计划,以检测食品动物中非法使用或滥用授权兽药的情况。这些国家还必须调查残留物违规的原因。向欧盟出口食品的非欧盟国家也必须实施残留物监测计划,以保证同等水平的食品安全。
因此,需要开发一种简单而准确的方法来测定海产品中各种抗生素的残留量。本应用纪要介绍了成功验证Waters ACQUITY UPLC I-Class PLUS系统与Xevo TQ-S micro质谱仪联用分析虾组织中四环素、磺胺类药物、甲氧苄氨嘧啶、奥美普林和氨苯砜的结果。
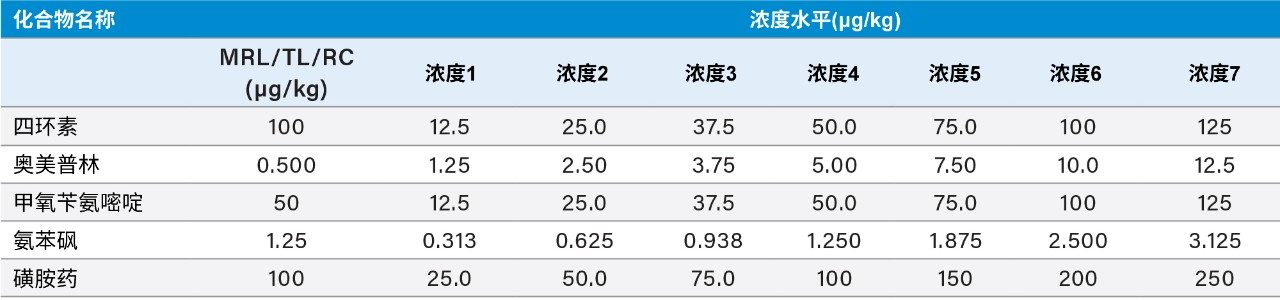
添加内标后,使用螯合剂混合物提取虾组织以提高四环素的提取效率,然后进行SPE净化(更多信息参见图1)。用虾组织提取物(之前显示为空白)制备基质匹配标准品,浓度如下(表1):

|
系统: |
配备FTN样品管理器的ACQUITY UPLC I-Class PLUS |
|
色谱柱: |
ACQUITY HSS C18, 1.8 μm, 2.1 × 100 mm(部件号:186003533) |
|
柱温: |
25 °C |
|
样品温度: |
10 °C |
|
进样参数: |
1 μL |
|
流动相A: |
水+0.1%甲酸 |
|
流动相B: |
甲醇 + 0.1%甲酸 |
|
样品管理器清洗液: |
25/25/25/25水/甲醇/异丙醇/乙腈,含0.2%甲酸 |
|
MS系统: |
Xevo TQ-S micro |
|
极性: |
ESI+ |
|
毛细管电压: |
2.0 kV |
|
离子源温度: |
150 °C |
|
脱溶剂气温度: |
650 °C |
|
脱溶剂气流速: |
1000 L/h |
|
锥孔气流速: |
50 L/h |
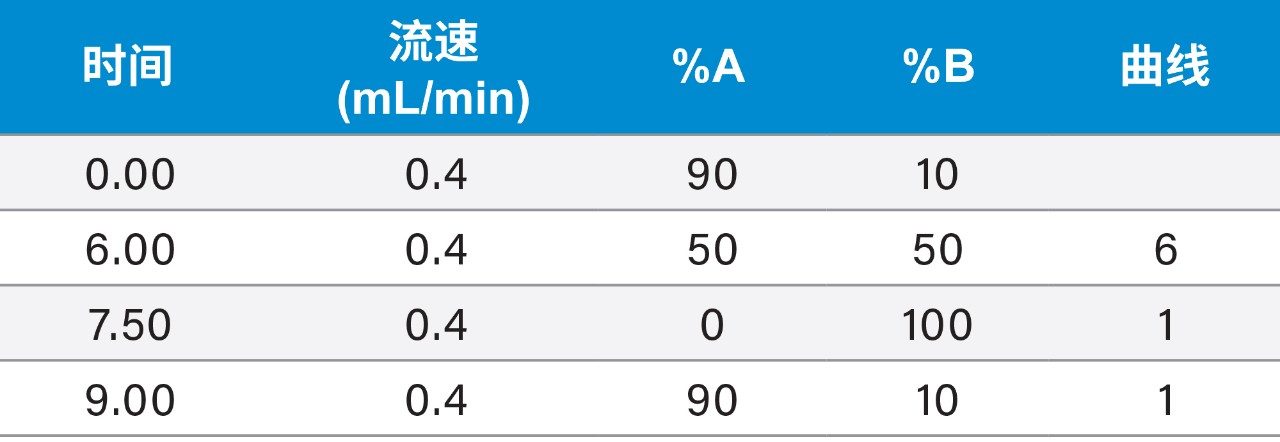
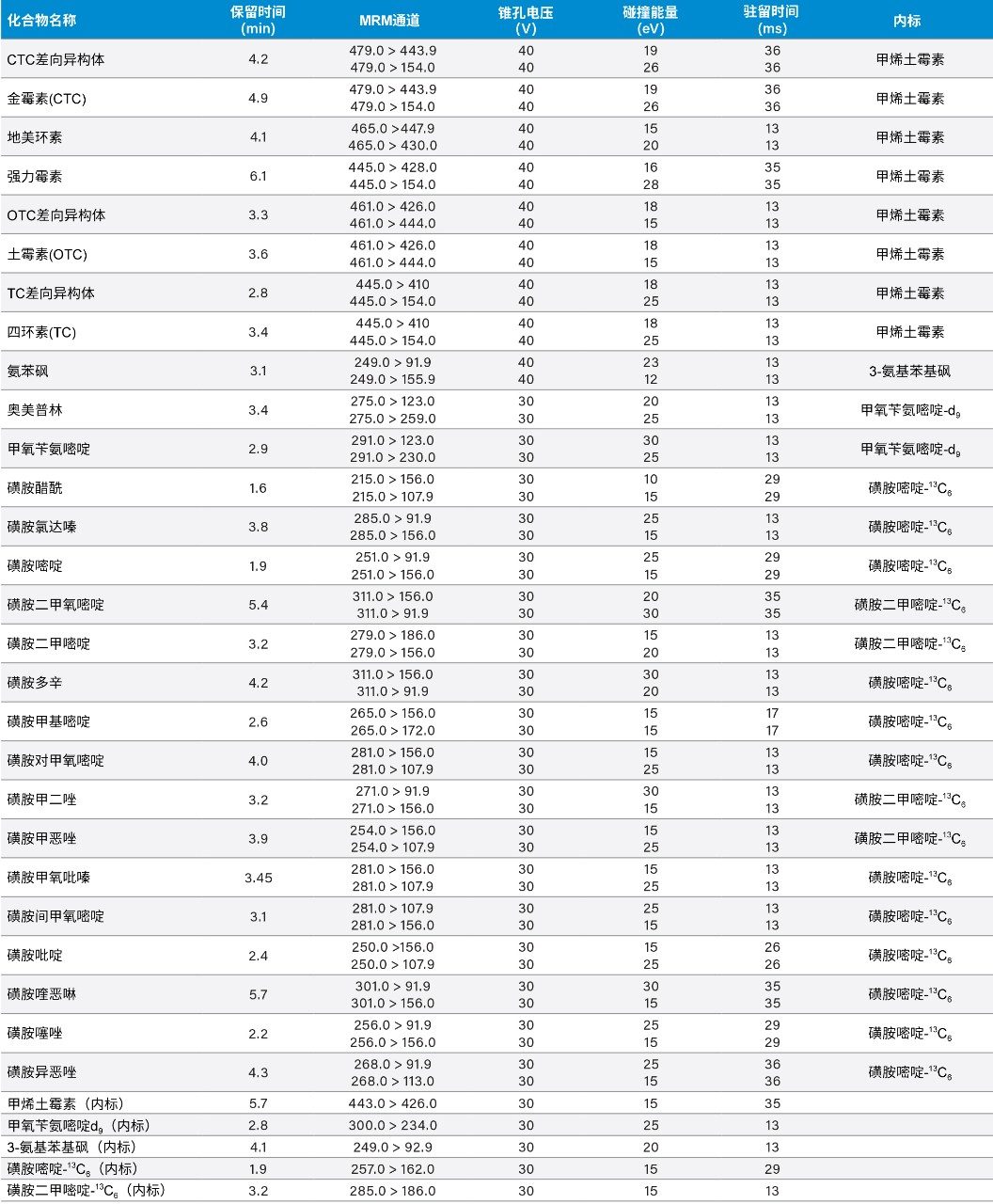
每种化合物采用两个MRM通道。利用Autodwell功能自动设置驻留时间,使每个峰至少包含12个数据点。利用MassLynx软件采集数据,并用TargetLynx XS应用软件进行处理。表2总结了MRM通道和实际驻留时间设置。定量迹线以粗体显示。
依据2002/657/EC指导原则,使用加标空白样品进行方法验证4。评估以下参数:鉴定结果、选择性、线性、正确度、实验室内重复性(RSDr)、实验室内重现性(RSDRL)、决定限度(CCα)和检出容量(CCβ)。通过检查保留时间、离子丰度比和鉴定点来评估鉴定结果。通过检测空白虾组织样品在分析物保留时间及附近是否有任何干扰物来验证方法选择性。对曲线的线性和各个残差进行检查。制备虾组织的重复加标样品,并由同一分析人员在三天内分别进行分析。对于规定了MRL的物质,样品中的加标量为MRL的0.5、1.0和1.5倍(见表1)。但是,由于四环素的MRL与母体药物及其4-差向异构体的总和有关,因此各化合物的加标浓度减半至25、50和75 μg/kg,并且在计算验证参数之前,首先对计算出的母体药物和差向异构体的浓度求和。对于未规定MRL的化合物,则以目标含量(TL)的0.5、1.0和1.5倍进行评估。CCα和CCβ依据2002/657/EC中定义的RSDRL进行计算。
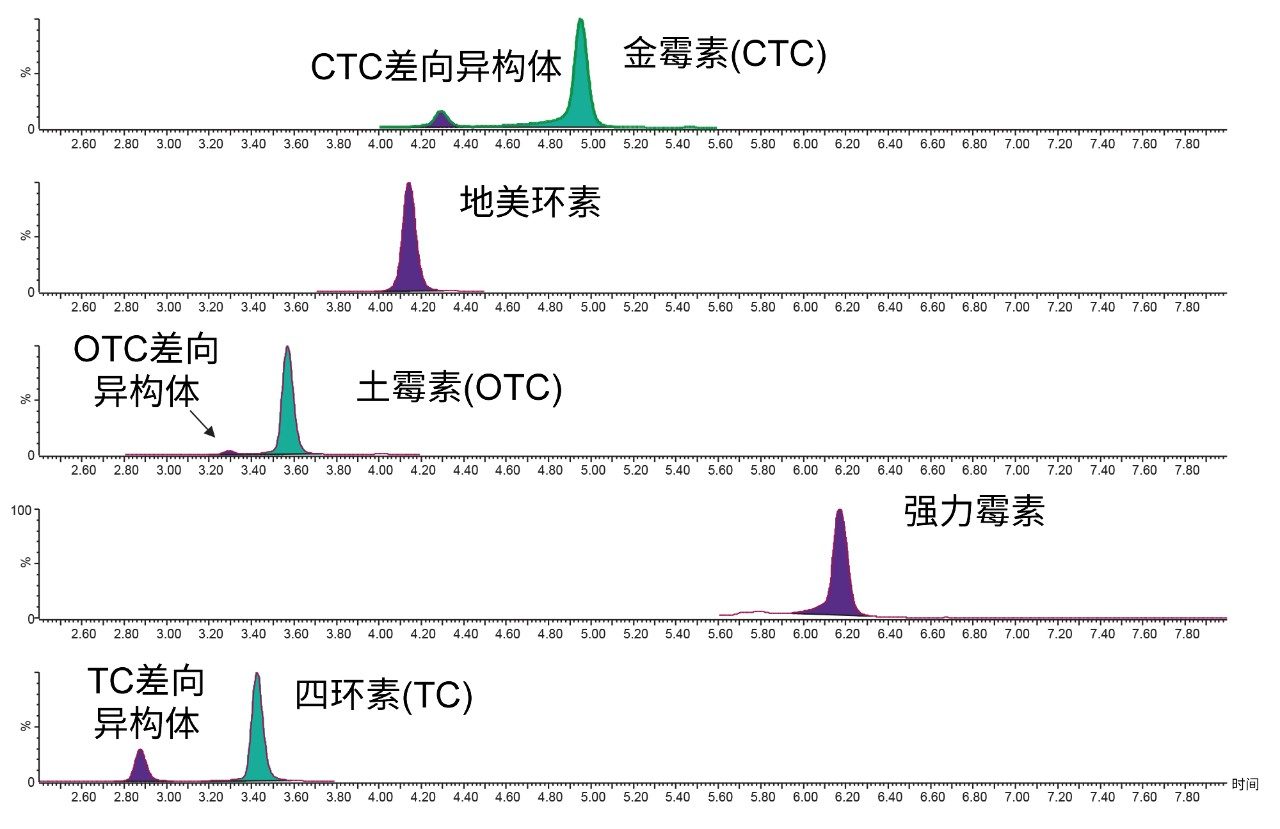
HSS C18色谱柱为所有分析物提供了优异的保留性能和峰形,在四环素分析中,无需向流动相中添加离子对试剂5。 HSS C18色谱柱结合甲醇(而不是乙腈)和低柱温条件,使母体药物及其差向异构体得到完全分离(图2)。
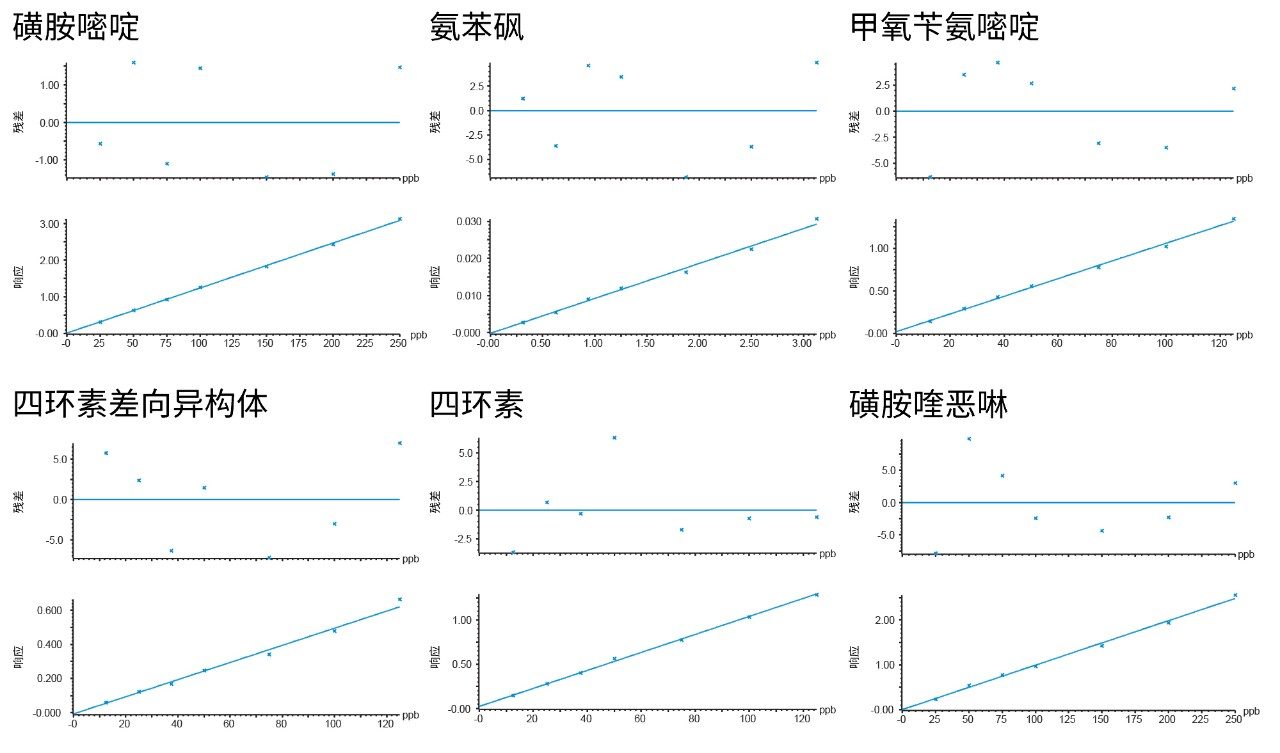
在三天内每天制备七个空白虾样品并进行分析。在提取物中未检测到可能导致误报不合规样品的信号。检测到一些痕量水平的化合物,但估计其浓度远低于最低浓度的标准品。利用基质提取物绘制7点校准曲线,每天采集一次数据。每种分析物采用两个通道足以满足所需的鉴定点(对于规定了MRL的物质为三个,对于违禁物为四个),所得峰的离子丰度比和保留时间均处于相较于标准品建议的偏差范围内。以1/x权重进行线性拟合,校准曲线的所有决定系数(R2)值均高于0.99,各个残差全都小于20%(大多数小于5%),表明定量结果可靠。典型校准曲线的一些示例如图3所示。
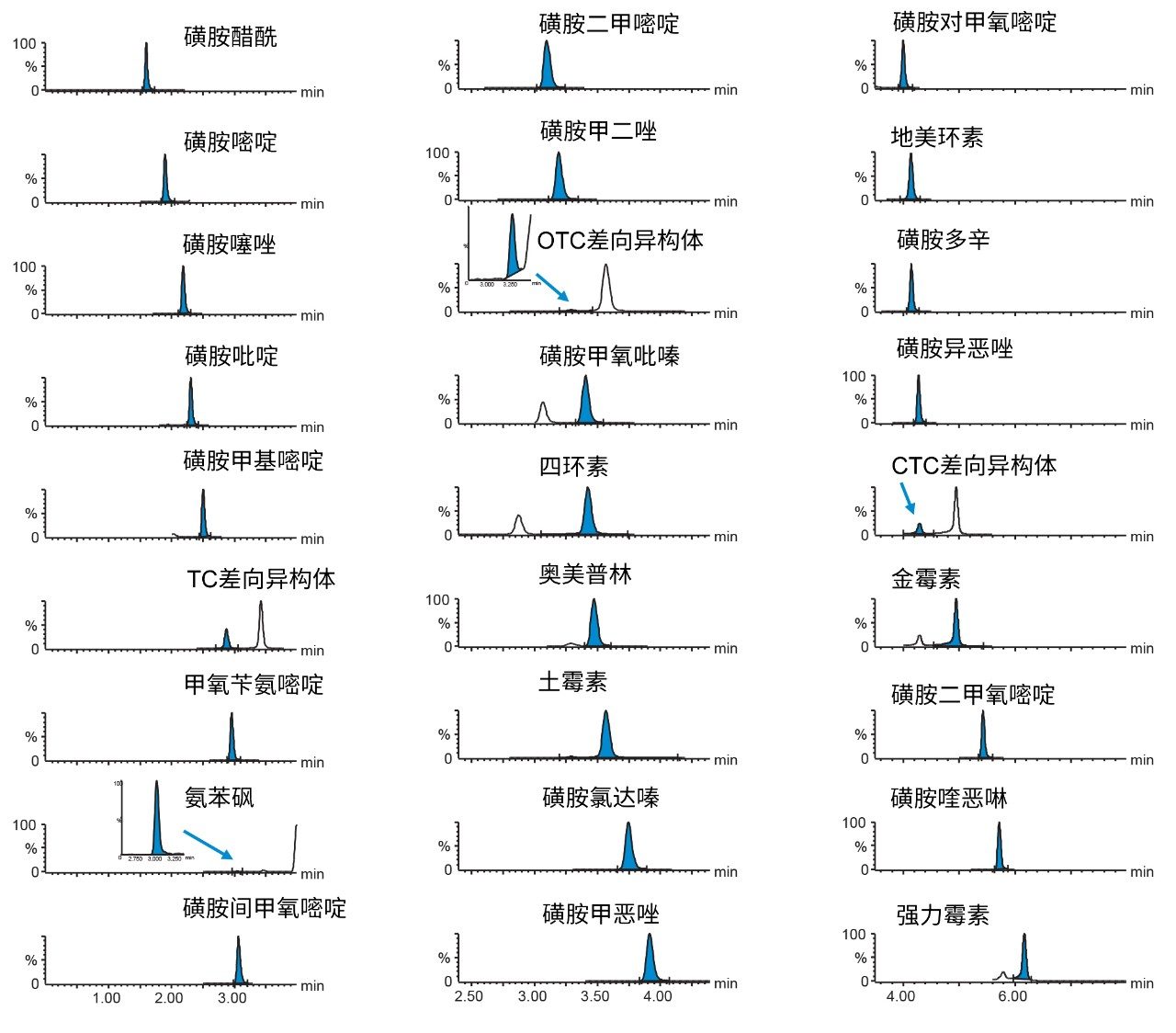
基质匹配标准品曲线的分析结果表明,该方法具有出色的灵敏度。图4所示为分析最低浓度的基质匹配标准品获得的一系列抗生素的典型色谱图,表明该方法能够检测提取物中更低浓度的这些抗生素,或者最终提取物可进一步稀释后再进行LC-MS/MS分析。
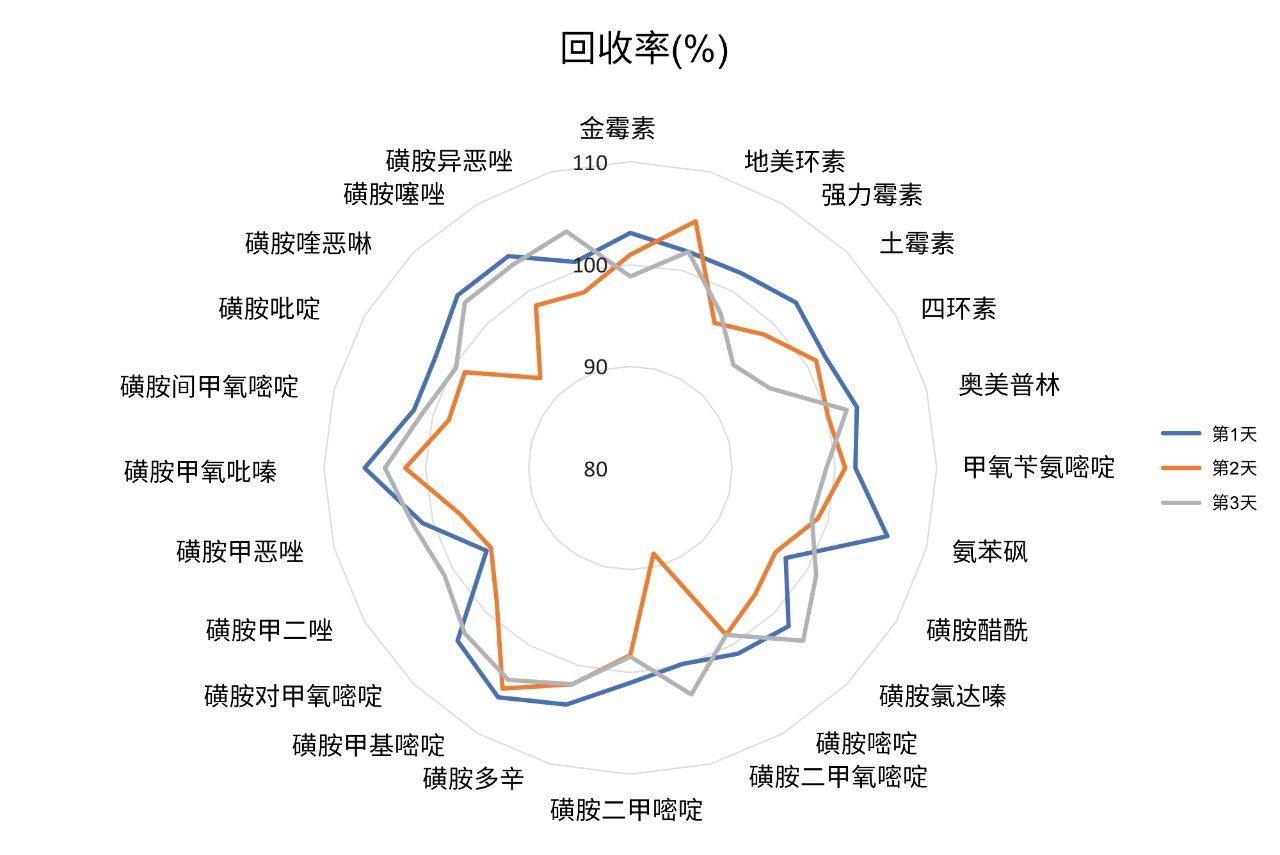
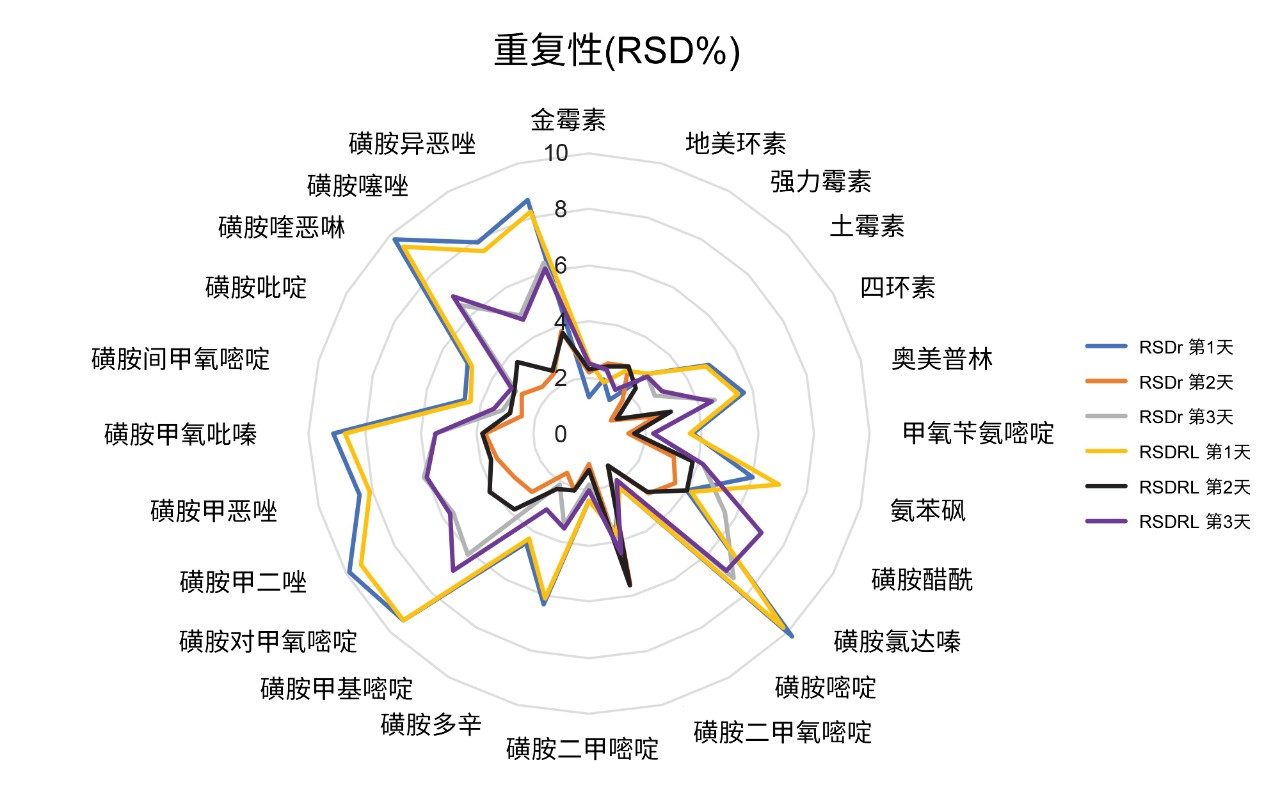
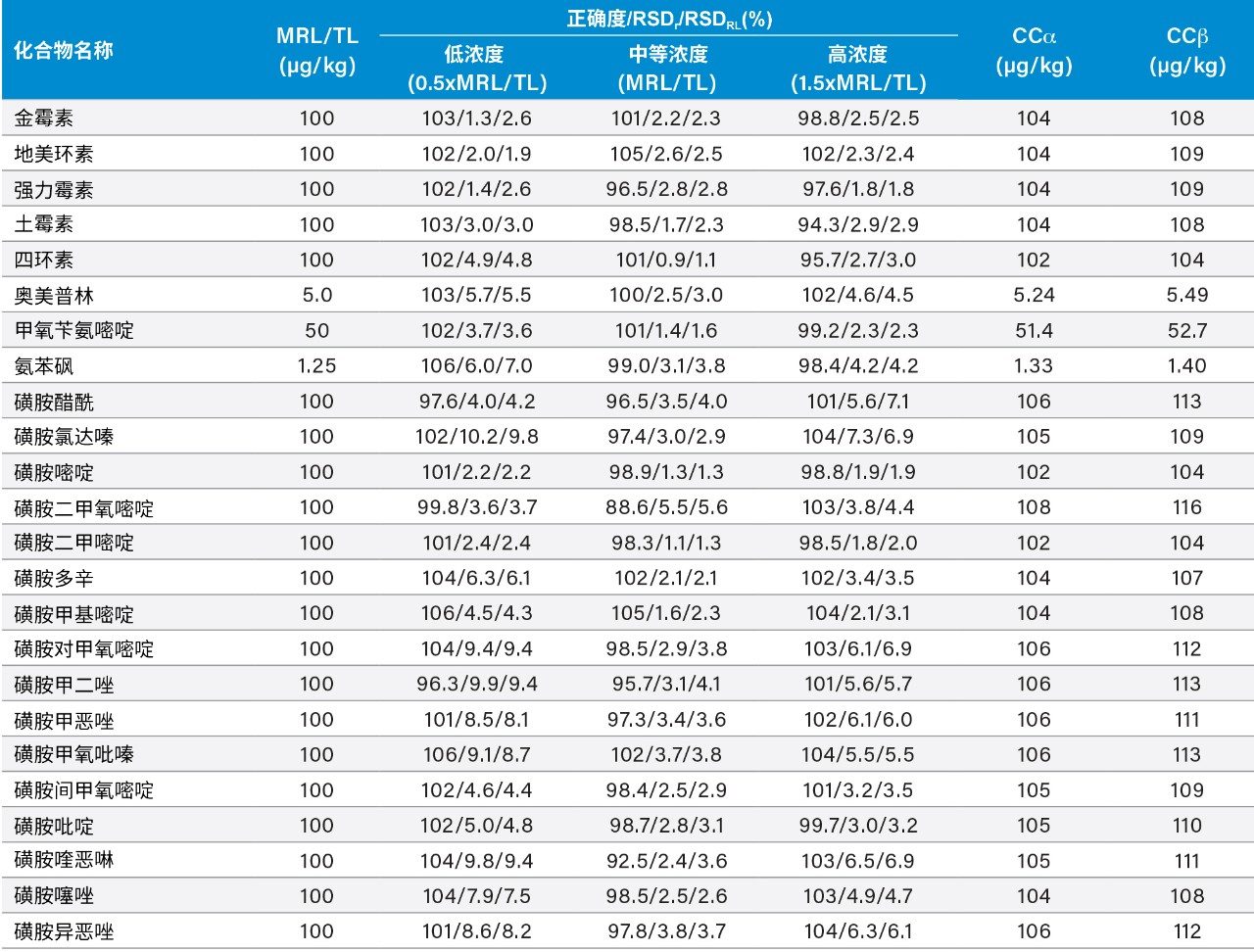
使用三天内分析加标样品得到的数据评估正确度,以实测回收率表示。在三天内制备三种浓度的加标样品,每组七个,并进行分析,所得回收率均在88.6%~106%的范围内。因此,符合欧盟委员会指令2002/657/EC中规定的标准。在RSDr (0.9%~10.2%)和RSDRL (1.1%~9.8%)研究中,该方法对所有分析物的重复性也令人满意。正确度和重复性结果见图5、图6和表3,表中还列出了CCα和CCβ值。
经证明,本文所述的使用ACQUITY UPLC I-Class PLUS与Xevo TQ-S micro MS/MS联用系统测定一系列不同抗生素(即四环素、磺胺类药物、甲氧苄氨嘧啶、奥美普林和氨苯砜抗生素)的方法是一种灵敏且稳定的多残留分析方法。该方法能够快速可靠地对浓度远低于典型MRL的分析物进行定量分析,并依据欧盟委员会指令2002/657成功验证,在对虾组织中四环素、磺胺类药物和相关抗生素的分析中提供了令人满意的结果。经适当验证后,该方法也可用于其他动物和鱼类组织的分析。这种经济有效的方法可在常规检测实验室中轻松实施,经证明适用于检查是否符合MRL规定,此外还有望用于筛查更低浓度的样品,例如用于食品生产商的尽职调查检测。
720006789ZH,2020年10月修订